题目内容
9.关于金属的下列说法错误的是( )| A. | 钠在空气中燃烧时,先熔化,再燃烧,最后所得产物为Na2O2 | |
| B. | 一定条件下,铁粉可与水蒸气反应 | |
| C. | 铝因在空气中形成的一薄层致密氧化膜对铝有保护作用,使得性质比较活泼的金属铝成为一种应用广泛的金属材料 | |
| D. | 铝与氢氧化钠溶液反应,氢氧化钠和水都是氧化剂 |
分析 A.钠的熔点较低,钠在空气中燃烧生成过氧化钠;
B.加热时Fe与水蒸气反应;
C.铝和氧气反应生成一层致密是氧化物薄膜,阻止进一步反应;
D.反应的本质是铝先和水反应生成氢气和氢氧化铝.
解答 解:A.钠的熔点较低,所以在空气燃烧时先熔化,再燃烧,燃烧时生成淡黄色的Na2O2,故A正确;
B.加热时Fe与水蒸气反应生成四氧化三铁和氢气,故B正确;
C.铝是亲氧元素,极易在空气中形成了一薄层致密的氧化膜阻止了铝进一步反应,从而保护内层金属,故铝不需特殊保护,故C正确;
D.反应的本质是铝先和水反应生成氢气和氢氧化铝,氢氧化铝再与氢氧化钠反应,故水是氧化剂,氢氧化钠不是氧化剂,故D错误;
故选D.
点评 本题考查金属的性质、氧化还原反应中氧化剂、还原剂的判断,明确反应中元素的化合价变化即可解答,注意把握铝在空气中不需要特殊保护的原因,题目难度不大.

练习册系列答案
相关题目
19.如表实验操作中,可达到对应实验目的是( )
| 实验操作 | 实验目的 | |
| A | 苯和溴水混合后加入铁粉 | 制溴苯 |
| B | 某有机物与溴的四氯化碳溶液混合 | 确认该有机物含碳碳双键 |
| C | 乙醇与高锰酸钾酸性溶液混合 | 乙醇具有还原性 |
| D | 将溴乙烷与氢氧化钠水溶液共热一段时间,冷却,向其中滴加硝酸银溶液 | 检验溴乙烷中的溴原子 |
| A. | A | B. | B | C. | C | D. | D |
20.在硫酸铁溶液中,加入a g铜,完全溶解后,又加入b g铁,充分反应后得到c g残余固体,且c<a,则下列判断正确的是( )
| A. | 最后得到的溶液中可能有Fe3+ | B. | 残余固体一定全部是铜 | ||
| C. | 最后得到的溶液中只含Cu2+ | D. | 残余固体可能为铁、铜混合物 |
17.维生素能使Fe3+转变成Fe2+,说明维生素C 具有( )
| A. | 氧化性 | B. | 还原性 | C. | 酸性 | D. | 碱性 |
14.一定质量的镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.下列关于反应的说法错误的是( )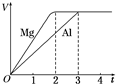

| A. | 镁和铝的物质的量之比为3:2 | B. | 镁和铝转移电子数之比为1:1 | ||
| C. | 镁和铝的摩尔质量之比为8:9 | D. | 镁和铝反应所用时间之比为3:2 |
1.下列有关实验操作、现象和解释或结论都正确的是
( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 某钠盐溶于盐酸,产生气体 | 使澄清石灰水变浑浊 | 说明该钠盐一定是Na2CO3 |
| B | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+,无K+ |
| C | 等物质的量浓度NaHCO3和Na2CO3与等浓度的稀盐酸反应 | NaHCO3更剧烈 | HCO3-结合H+的能力比CO32-结合H+的能力强 |
| D | 向AlCl3溶液中加放足量的氨水 | 有白色沉淀产生且白色沉淀不消失 | 氨水呈弱碱性 |
| A. | A | B. | B | C. | C | D. | D |
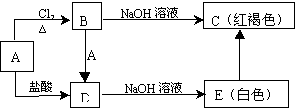
 该物质能使酸性KMnO4溶液褪色,在这个反应中体现了该物质的还原性(填“氧化性”或“还原性”).
该物质能使酸性KMnO4溶液褪色,在这个反应中体现了该物质的还原性(填“氧化性”或“还原性”).