题目内容
16.短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是电子层数的三倍,Y与X可形成Y2X2和Y2X两种离子化合物,Z原子的核外电子数比Y原子多1,W与X同主族,则( )| A. | 原子半径:Y<Z<W | |
| B. | 单质的还原性:Y>Z | |
| C. | 气态氢化物的稳定性:X<W | |
| D. | Y和Z两者最高价氧化物对应的水化物能相互反应 |
分析 短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是电子层数的三倍,最外层电子数不超过8个,K层不超过2个;Y与X可形成Y2X2和Y2X两种离子化合物,则X为O元素,Y为Na元素;
Z原子的核外电子数比Y原子多1,则Z为Mg元素;
W与X同主族,则W为S元素;
A.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
B.元素的金属性越强,其单质的还原性越强;
C.元素的非金属性越强,其氢化物的稳定性越强;
D.Y、Z元素最高价氧化物的水化物分别是NaOH、Mg(OH)2,两性氢氧化物能溶于强酸强碱.
解答 解:短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是电子层数的三倍,最外层电子数不超过8个,K层不超过2个;Y与X可形成Y2X2和Y2X两种离子化合物,则X为O元素,Y为Na元素;
Z原子的核外电子数比Y原子多1,则Z为Mg元素;
W与X同主族,则W为S元素;
A.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径Na>Mg>S>O,即Y>Z>W,故A错误;
B.元素的金属性越强,其单质的还原性越强,金属性Y>Z,所以单质的还原性Y>Z,故B正确;
C.元素的非金属性越强,其氢化物的稳定性越强,非金属性X>W,所以氢化物的稳定性X>W,故C错误;
D.Y、Z元素最高价氧化物的水化物分别是NaOH、Mg(OH)2,两性氢氧化物能溶于强酸强碱,氢氧化镁没哟两性,所以不能溶于氢氧化钠溶液,故D错误;
故选B.
点评 本题考查原子结构和元素周期律关系,为高考高频点,明确同一周期、同一主族性质递变规律即可解答,知道金属性、非金属性强弱判断方法,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
7.下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①N,⑤Si,⑦C.
(2)画出原子的结构示意图:④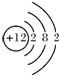 ,⑥
,⑥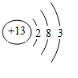 ,⑧
,⑧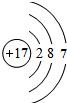 .
.
(3)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar.
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应: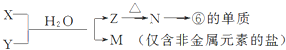
X溶液与Y溶液反应的离子方程式为Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$,
N→⑥的单质的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑,
(6)在③与④中,化学性质较活泼的是Na,怎样用化学实验证明?
答:与水反应;
在⑧与⑫中,化学性质较活泼的是Cl2,请用化学方程式来说明.
答:Cl2+2NaBr=2NaCl+Br2.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ⑬ | |||||||
| 2 | ① | ⑭ | ② | |||||
| 3 | ③ | ④ | ⑥ | ⑤ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)画出原子的结构示意图:④
 ,⑥
,⑥ ,⑧
,⑧ .
.(3)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar.
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
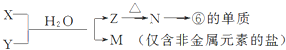
X溶液与Y溶液反应的离子方程式为Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$,
N→⑥的单质的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑,
(6)在③与④中,化学性质较活泼的是Na,怎样用化学实验证明?
答:与水反应;
在⑧与⑫中,化学性质较活泼的是Cl2,请用化学方程式来说明.
答:Cl2+2NaBr=2NaCl+Br2.
4.下列保存物质的方法正确的是( )
| A. | 液氯贮存在干燥的钢瓶里 | |
| B. | 少量的锂、钠、钾均保存在煤油中 | |
| C. | 浓溴水保存在带橡皮塞的棕色细口瓶中 | |
| D. | 用排水法收集满一瓶氢气,用玻璃片盖住瓶口,瓶口朝上放置 |
1.已知醇之间发生反应:R-OH+H-OR′$→_{△}^{浓硫酸}$R-O-R′(醚)+H2O,由两种不同的醇反应得到某醚M为C5H11OC5H11,它代表了多少种物质( )
| A. | 28 | B. | 36 | C. | 64 | D. | 48 |
8.下列实验可行的是( )
| A. | 用NaOH溶液除去CO2中混有的HCl气体 | |
| B. | 加入适量铜粉除去Cu(NO3)2溶液中的AgNO3杂质 | |
| C. | 所有不锈钢都只含有金属元素 | |
| D. | 用乙醇从碘水中萃取碘 |