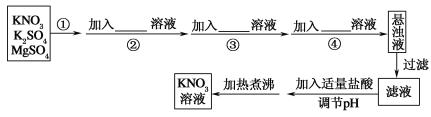
��Ŀ����
����Ŀ���ں��º��ݵ������У�������Ӧ��H2(g)+CO(g)![]() C(s)+H2O(g)����ʼʱ����ƽ����Է�������Ϊ15��H2��CO�������һ��ʱ����������ƽ����Է�������Ϊ16������˵���в���ȷ����( )
C(s)+H2O(g)����ʼʱ����ƽ����Է�������Ϊ15��H2��CO�������һ��ʱ����������ƽ����Է�������Ϊ16������˵���в���ȷ����( )
A����Ӧǰ�������ѹǿ֮��Ϊ4��3
B����Ӧǰ��������ܶ�֮��Ϊ15��16
C��H2��CO��ת������ȣ���Ϊ50%
D����H2��CO��8��5����Ȼ�ϣ���Ӧǰ���������ƽ����Է�����������
���𰸡�B
��������
�����������ʼʱƽ��������Ϊ15������ʮ�ֽ��淨��(28��15)/(15��2)=1��1������ʼͶ������ͬ���迪ʼʱͶ��1mol����
H2(g)��CO(g)![]() C(s)��H2O(g)
C(s)��H2O(g)
��ʼ��mol���� 1 1 0
���ģ�mol���� x x x
һ��ʱ�䣨mol����1��x 1��x x
����Ħ�������Ķ��壬[2(1��x)��28(1��x)��18x]/(1��x��1��x��x)=16�����x=0.5mol��A��ѹǿ֮�ȵ������ʵ���֮�ȣ���2����2��0.5��=4��3��A��ȷ��B�������ܶȵĶ��壬���ǵ��ݣ���������ͬ���ܶ�֮�ȵ�������֮�ȣ�30��24=15��12��B����C�����������жϣ�ת����Ϊ![]() ��100%=50%��C��ȷ��D����H2��CO��8��5����Ȼ�ϣ���
��100%=50%��C��ȷ��D����H2��CO��8��5����Ȼ�ϣ���
H2(g)��CO(g)![]() C(s)��H2O(g)
C(s)��H2O(g)
��ʼ��mol���� 8n 5n 0
������mol���� y y y
һ��ʱ����mol����8n��y 5n��y y
���ջ�������ƽ����Է���������![]() ������Ӧǰ�������Է���������
������Ӧǰ�������Է���������![]() ��D��ȷ����ѡB��
��D��ȷ����ѡB��