题目内容
下列说法正确的是
| A.常温下,向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,则常温下Ksp (BaCO3)<Ksp (BaSO4) |
| B.常温下,向纯水中加入钠或氢氧化钠都能使水的电离平衡逆向移动,水的离子积不变 |
| C.常温下,反应4Fe(OH)2(s)+ O2(g) +2H2O(l) =4Fe(OH)3(s)的△H<0、△S<0 |
| D.铅蓄电池在工作过程中,负极质量减少,阳极质量增加 |
C
A.不符合客观事实,Ksp (BaCO3)>Ksp (BaSO4) ;
B.钠和水反应,放出大量的热,温度升高,水的离子积增大;
D.铅蓄电池在工作过程中,负极质量减少,正极质量增加
B.钠和水反应,放出大量的热,温度升高,水的离子积增大;
D.铅蓄电池在工作过程中,负极质量减少,正极质量增加

练习册系列答案
相关题目
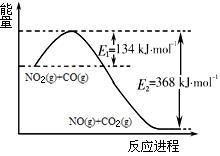
 2NH3(g) △H < 0 ,其平衡常数K与温度T的关系如下表:
2NH3(g) △H < 0 ,其平衡常数K与温度T的关系如下表: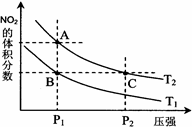
 2B(g);△H,若正反应的活化能为Ea kJ mol-1,逆反应的活化能为Eb kJ·mol-1,则△H=(Ea-Eb)kJ·mol-1
2B(g);△H,若正反应的活化能为Ea kJ mol-1,逆反应的活化能为Eb kJ·mol-1,则△H=(Ea-Eb)kJ·mol-1
 的焓变为ΔH = -384 kJ·mol-1
的焓变为ΔH = -384 kJ·mol-1
 2NH3(g) ΔH <0。400℃时,K= 0.5,某一时刻测得N2、H2和NH3三种物质物质的量分别为2mol、1mol和3mol,则该反应的v正(N2) v逆(N2)(填 “>” 、“="”" 或 “<”)
2NH3(g) ΔH <0。400℃时,K= 0.5,某一时刻测得N2、H2和NH3三种物质物质的量分别为2mol、1mol和3mol,则该反应的v正(N2) v逆(N2)(填 “>” 、“="”" 或 “<”) 浓度mol.L-1
浓度mol.L-1 2NH3(g)+ O2(g)。回答下列问题:
2NH3(g)+ O2(g)。回答下列问题:

 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
