题目内容
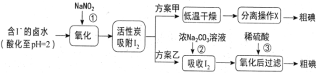
【题目】MnCO3可用于制备活性电极材料MnO2。以菱锰矿(含MnCO3、SiO2、FeCO3和少量Al2O3等)为原料制备碳酸锰粗产品的流程如下:

已知:①常温下,Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=4.0×10-34。
②氢氧化物沉淀的条件:Al3+、Fe3+完全沉淀的pH分别为4.6、3.4;Mn2+开始沉淀的pH为8.1。
(1)“酸浸”过程中不能用浓盐酸替代硫酸,原因是_________________________________。
(2)用离子方程式表示“氧化”过程中加MnO2的目的:______________________________。
(3)“调pH”时,向含有硫酸铁和硫酸铝的混合溶液中滴加氢氧化钠溶液至两种沉淀共存,当c(Fe3+)=1.0×10-5mol·L-1时,c(Al3+)=______________mol·L-1。
(4)①“沉锰”过程中,反应的离子方程式为__________________________________。
②“沉锰”过程中沉锰速率与温度的关系如图所示。
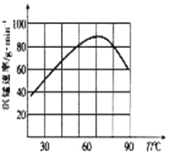
当温度高于60℃时,沉锰速率随着温度升高而减慢的原因可能是___________________。
(5)从滤液3中可分离出一种不含碳元素的氮肥,它的化学式为___________________。
【答案】 后续“氧化”过程中加入的二氧化锰会氧化浓盐酸 MnO2+2Fe2++4H+===Mn2++2Fe3++2H2O 0.05 Mn2++2HCO3-===MnCO3↓+CO2↑+H2O 温度过高时碳酸氢铵的分解速率显著加快,沉锰速率随碳酸氢铵浓度的减小而减慢 (NH4)2SO4
【解析】(1)浓盐酸具有还原性,后续“氧化”过程中会加入二氧化锰,二氧化锰可以氧化浓盐酸,因此“酸浸”过程中不能用浓盐酸替代硫酸;(2)在强酸性条件下,MnO2将Fe2+氧化为更容易转化为氢氧化物沉淀的Fe3+:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;(3)当Fe(OH)3和Al(OH)3两种沉淀共存时,有Fe3++ Al (OH)3=Al3++Fe(OH)3,故c(Al3+)=![]() =
=![]() =0.05 mol·L-1;(4)①沉锰过程中有MnCO3沉淀和CO2气体生成,故反应的离子方程式为Mn2++2HCO3-=MnCO3↓+CO2↑+H2O;②温度高于60 ℃时,继续升温,碳酸氢铵的分解速率显著加快,沉锰速率随碳酸氢铵浓度的减小而减慢;(5)“酸浸”时引入了SO42-,“沉锰”时引入了NH4+,故滤液3中可分离出的一种不含碳元素的氮肥是(NH4)2SO4。
=0.05 mol·L-1;(4)①沉锰过程中有MnCO3沉淀和CO2气体生成,故反应的离子方程式为Mn2++2HCO3-=MnCO3↓+CO2↑+H2O;②温度高于60 ℃时,继续升温,碳酸氢铵的分解速率显著加快,沉锰速率随碳酸氢铵浓度的减小而减慢;(5)“酸浸”时引入了SO42-,“沉锰”时引入了NH4+,故滤液3中可分离出的一种不含碳元素的氮肥是(NH4)2SO4。

 名校课堂系列答案
名校课堂系列答案