题目内容
【题目】设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.2gD2中所含的电子的数目为2NA
B.标况下4.48L CHCl3中所含的原子数目为NA
C.4.4g CO2中所含的共用电子对数目为0.2NA
D.14 g乙烯和环己烷( ![]() )的混合物中,所含碳原子数为NA
)的混合物中,所含碳原子数为NA
【答案】D
【解析】A.n= ![]() 计算物质的量=
计算物质的量= ![]() =0.5mol,D2分子中含2个电子,2gD2中所含的电子的数目=0.5mol×2×NA=NA,A不符合题意;
=0.5mol,D2分子中含2个电子,2gD2中所含的电子的数目=0.5mol×2×NA=NA,A不符合题意;
B.标准状况下三氯甲烷不是气体,标况下4.48L CHCl3物质的量不是0.2mol,B不符合题意;
C.n= ![]() 计算物质的量=
计算物质的量= ![]() =0.1mol,一个二氧化碳分子中含共用电子对数为四个,4.4g CO2中所含的共用电子对数目为0.4NA,C不符合题意;
=0.1mol,一个二氧化碳分子中含共用电子对数为四个,4.4g CO2中所含的共用电子对数目为0.4NA,C不符合题意;
D.乙烯和环己烷( ![]() )的最简式相同为CH2,计算14 gCH2中所含碳原子数=
)的最简式相同为CH2,计算14 gCH2中所含碳原子数= ![]() ×NA=NA,D符合题意;
×NA=NA,D符合题意;
所以答案是:D.

【题目】实验室制备1,2﹣二溴乙烷的反应原理如下:
CH3CH2OH 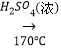 CH2=CH2
CH2=CH2
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚.
用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如图所示:
有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | ﹣116 |
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 , 其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)若产物中有少量副产物乙醚.可用的方法除去;
(4)反应过程中应用冷水冷却装置D,其主要目的是避免溴大量挥发,但又不能过度冷却(如用冰水),其原因是 .