题目内容
【题目】下列反应的离子方程式,正确的是( )
A.用小苏打治疗胃酸过多:CO ![]() +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
B.AlCl3溶液中加入足量的氨水:Al3++3OH﹣═Al(OH)3↓
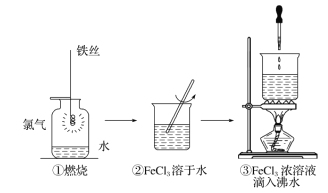
C.用FeCl3溶液腐蚀印刷电路板上铜箔:Fe3++Cu═Fe2++Cu2+
D.铝与浓氢氧化钠溶液反应:2Al+2OH﹣+2H2O═2AlO ![]() +3H2↑
+3H2↑
【答案】D
【解析】解:A.用小苏打治疗胃酸过多的离子反应为HCO ![]() +H+═CO2↑+H2O,故A错误; B.AlCl3溶液中加入足量的氨水的离子反应为Al3++3NH3 . H2O═Al(OH)3↓+3NH
+H+═CO2↑+H2O,故A错误; B.AlCl3溶液中加入足量的氨水的离子反应为Al3++3NH3 . H2O═Al(OH)3↓+3NH ![]() ,故B错误;
,故B错误;
C.FeCl3溶液腐蚀印刷电路板上铜箔的离子反应为2Fe3++Cu═2Fe2++Cu2+ , 故C错误;
D.铝与浓氢氧化钠溶液反应的离子反应为2Al+2OH﹣+2H2O═2AlO ![]() +3H2↑,故D正确;
+3H2↑,故D正确;
故选D.

【题目】根据题意填空
(1)有一学生在实验室测某溶液pH.实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测.
①这种错误操作(填“一定”/“一定不”/“不一定”)会导致实验结果有误差.
②若按此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 .
(2)用已知浓度的 NaOH 溶液测定某 HCl溶液的浓度,参考如图,从表中选出正确序号
序号 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 |
|
A | 碱 | 酸 | 石芯 | (乙) |
B | 酸 | 碱 | 酚酞 | (甲) |
C | 碱 | 酸 | 甲基橙 | (甲) |
D | 酸 | 碱 | 酚酞 | (乙) |
(3)用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管.