题目内容
【题目】常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA﹣ , Ⅲ代表A2﹣)所示.根据图示判断,下列说法正确的是( ) 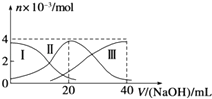
A.当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA﹣)>c(A2﹣)>c(H+)>c(OH﹣)
B.等浓度的NaOH溶液与H2A溶液按2:1混合后,其溶液中水的电离程度比纯水小
C.NaHA溶液中:c(OH﹣)+c(A2﹣)=c(H+)+c(H2A)
D.向上述加入20mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减少
【答案】C
【解析】解:A.根据图象知,当V(NaOH)=20 mL时,发生反应为NaOH+H2A═NaHA+H2O,溶质主要为NaHA,HA﹣电离程度大于水解程度,溶液显酸性,水和HA﹣都电离出氢离子,只有HA﹣电离出A2﹣ , 所以离子浓度大小顺序是c(Na+)>c(HA﹣)>c(H+)>c(A2﹣)>c(OH﹣),故A错误;
B.等浓度的NaOH溶液与H2A溶液按体积2:1混合后,二者恰好反应生成Na2A和水,Na2A是强碱弱酸盐促进水电离,故B错误;
C.根据电荷守恒得c(OH﹣)+2c(A2﹣)+c(HA﹣)=c(H+)+c(Na+),根据物料守恒得c(Na+)=c(HA﹣)+c(H2A)+c(A2﹣),所以得c(OH﹣)+c(A2﹣)=c(H+)+c(H2A),故C正确;
D.二者恰好反应生成NaHA,此时溶液呈酸性,加水稀释显性离子浓度变小,隐性离子氢氧根离子浓度增大,所以pH增大,故D错误;
故选:C.

【题目】高锰酸钾[KMnO4]是常用的氧化剂.工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体.中间产物为锰酸钾[K2MnO4].图1是实验室模拟制备的操作流程: 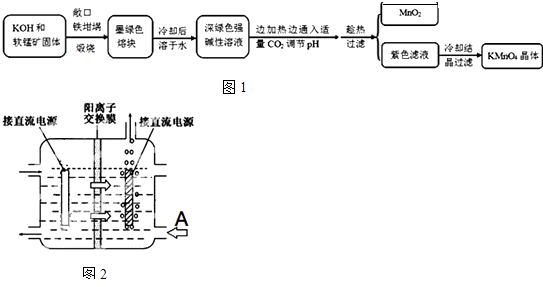
相关资料:
①物质溶解度
物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
②锰酸钾[K2MnO4]
外观性状:墨绿色结晶.其水溶液呈深绿色,这是锰酸根(MnO42﹣)的特征颜色.
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42﹣会发生歧化反应.
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是;
(2)实验时,若CO2过量会生成KHCO3 , 导致得到的KMnO4产品的纯度降低.请写出实验中通入适量CO2时体系中可能发生反应离子方程式:;
其中氧化还原反应中氧化剂和还原剂的质量比为 .
(3)由于CO2的通入量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸.从理论上分析,选用下列酸中 , 得到的产品纯度更高.
A.醋酸
B.浓盐酸
C.稀硫酸
(4)工业上采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图).图2中A口加入的溶液最好为 . 使用阳离子交换膜可以提高Mn元素利用率的原因为 .