题目内容
【题目】某学习小组探究SO2与Cu(OH)2悬浊液的反应。
实验Ⅰ:向NaOH溶液中加入浓CuCl2溶液,制得含Cu(OH)2的悬浊液,测溶液pH≈13。向悬浊液中通入SO2,产生大量白色沉淀,测溶液pH≈3。推测白色沉淀中可能含有Cu+、Cu2+、Cl- 、SO42-、SO32-、HSO3-。
已知: i. Cu(NH3)42+(蓝色);Cu+![]() Cu(NH3)2+(无色);Cu+
Cu(NH3)2+(无色);Cu+![]() Cu+Cu2+
Cu+Cu2+
ii. Ag2SO4微溶于水,可溶于一定浓度的硝酸。
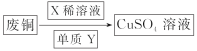
实验Ⅱ:

(1)①通过“白色沉淀A”确定一定存在的离子是____________________。
②判断白色沉淀中金属离子仅含有Cu+、不含Cu2+的实验证据是____________________。
③用以证实白色沉淀中无SO42-、SO32-、HSO3-的试剂a是____________________。
④生成CuCl的离子方程式是____________________。
(2)小组同学基于上述实验认为: SO2与Cu(OH)2悬浊液能发生氧化还原反应不仅基于本身的性质,还受到“生成了沉淀促进了氧化还原反应的发生”的影响。设计实验验证了此观点。
①用实验Ⅰ方法制得含Cu(OH)2的悬浊液,过滤、洗涤获取纯净的Cu(OH)2固体。检验Cu(OH)2固体是否洗涤干净的方法是____________________。
编号 | 实验 | 现象 |
III | 向Cu(OH)2固体中加入一定量的水,制得悬浊液(pH≈8),向悬浊液中通入SO2 | a. 底部产生少量浅黄色沉淀,慢慢消失 b. 静置,底部产生少量红色固体 |
IV | 向CuSO4溶液中通入SO2 | 无沉淀产生 |
②经确认浅黄色沉淀是CuOH,红色固体是Cu,证明SO2与Cu(OH)2悬浊液发生了氧化还原反应。最终生成Cu的原因是____________________。
③由实验III、IV可以得出的结论除“生成了沉淀促进了氧化还原反应的发生” 外还有____________________。
【答案】Cl- 白色沉淀溶于氨水后无色说明无Cu2+,后变成蓝色说明含 Cu+ 硝酸酸化的BaCl2[或Ba(NO3)2]溶液 SO2 + 2Cl-+2 Cu(OH)2 = 2CuCl + SO42- + 2H2O 用小试管接取最后的几滴洗涤液,加入(硝酸酸化的)AgNO3溶液,无沉淀产生 SO2 与Cu(OH)2 反应生成CuOH,过量SO2溶于水使溶液显酸性,CuOH在酸性溶液里反应最终生成Cu 和Cu2+ SO2与二价铜在碱性条件下更容易发生氧化还原反应
【解析】
(1)①根据实验Ⅱ可知,蓝色溶液中加入硝酸和硝酸银得到“白色沉淀A”,据此分析判断;②根据白色沉淀中加入氨水得到无色溶液,之后变成蓝色分析解答;③SO32-、HSO3-都能被硝酸氧化生成SO42-,结合硫酸根离子的检验方法分析解答;④根据实验Ⅱ可知,白色沉淀为CuCl,即实验I中生成的白色沉淀为CuCl,据此书写反应的离子方程式;
(2)①用实验Ⅰ方法制得含Cu(OH)2的悬浊液,过滤得到的Cu(OH)2固体上吸附了Cl-,据此分析解答;②浅黄色沉淀是CuOH,说明SO2与Cu(OH)2悬浊液发生了氧化还原反应,在过量SO2溶于水使溶液显酸性后,CuOH在酸性溶液里发生歧化反应,据此分析解答;③根据实验III、IV,比较溶液的酸碱性对实验的影响分析解答。
(1)①根据实验Ⅱ可知,蓝色溶液中加入硝酸和硝酸银得到“白色沉淀A”,A为AgCl,说明溶液中一定存在Cl-,故答案为:Cl-;
②白色沉淀中加入氨水得到无色溶液,说明无Cu2+,后变成蓝色说明含 Cu+,因此白色沉淀中金属离子仅含有Cu+、不含Cu2+,故答案为:白色沉淀溶于氨水后无色说明无Cu2+,后变成蓝色说明含 Cu+;
③SO32-、HSO3-都能被硝酸氧化生成SO42-,因此证实白色沉淀中无SO42-、SO32-、HSO3-的试剂a是硝酸酸化的BaCl2[或Ba(NO3)2]溶液,故答案为:硝酸酸化的BaCl2[或Ba(NO3)2]溶液;
④根据实验Ⅱ可知,白色沉淀为CuCl,即实验I中生成的白色沉淀为CuCl,反应的离子方程式为SO2 + 2Cl-+2 Cu(OH)2 = 2CuCl + SO42- + 2H2O,故答案为:SO2 + 2Cl-+2 Cu(OH)2 = 2CuCl + SO42- + 2H2O;
(2)①用实验Ⅰ方法制得含Cu(OH)2的悬浊液,过滤得到的Cu(OH)2固体上吸附了Cl-,洗涤获取纯净的Cu(OH)2固体,因此检验Cu(OH)2固体是否洗涤干净只需要检验洗涤后的滤液中是否含有Cl-,方法为:用小试管接取最后的几滴洗涤液,加入(硝酸酸化的)AgNO3溶液,无沉淀产生,说明沉淀已洗净,故答案为:用小试管接取最后的几滴洗涤液,加入(硝酸酸化的)AgNO3溶液,无沉淀产生;
②经确认浅黄色沉淀是CuOH,说明SO2与Cu(OH)2悬浊液发生了氧化还原反应。过量SO2溶于水使溶液显酸性,CuOH在酸性溶液里反应最终生成Cu 和Cu2+,因此红色固体是Cu,故答案为:SO2 与Cu(OH)2 反应生成CuOH,过量SO2溶于水使溶液显酸性,CuOH在酸性溶液里反应最终生成Cu 和Cu2+;
③根据实验III、IV可知SO2与二价铜在碱性条件下更容易发生氧化还原反应,故答案为:SO2与二价铜在碱性条件下更容易发生氧化还原反应。

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案【题目】下列实验操作能达到目的的是( )
选项 | 实验目的 | 实验操作 |
A | 配制100 g10%的NaOH溶液 | 称取10 gNaOH溶于90 g蒸馏水中 |
B | 验证“84消毒液”呈碱性 | 用pH试纸测量溶液的pH |
C | 检验溶液中是否含有Na+ | 用洁净的玻璃棒蘸取溶液灼烧,观察火焰颜色 |
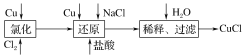
D | 从溴水中获得溴单质 | 利用SO2将Br2吹出后,富集、还原、分离 |
A.AB.BC.CD.D