题目内容
在相同温度下,100 mL0.01 mol·L-1的醋酸溶液与10 mL0.1 mol·L-1的醋酸溶液相比较,下列数值前者大于后者的是
| A.中和时所需NaOH的量 | B.电离的程度 |
| C.H+的物质的量浓度 | D.CH3COOH的物质的量 |
B
解析试题分析:100 mL0.01 mol·L-1的醋酸溶液与10 mL0.1 mol·L-1的醋酸溶液中所含醋酸的物质的量相等,所以中和时所需NaOH的量相等;H+的物质的量浓度后者大;电离程度前者大,弱电解质越稀越电离。正确答案B
考点:弱电解质溶液

练习册系列答案
相关题目
常温下,将pH和体积都相同的盐酸和醋酸溶液分别加蒸馏水稀释,pH随溶液体积变化如图,下列有关叙述正确的是
| A.曲线I为醋酸稀释时pH值变化曲线 |
| B.a点时,若都加入相同大小的锌粒,此时盐酸反应的速率大 |
| C.a点时,若都加入足量的锌粒,最终与醋酸反应产生的氢气多 |
| D.b点溶液中水的电离程度比c点溶液中水的电离程度小 |
下列物质的水溶液, pH>7的是
| A.NH4HSO4 | B.NaHCO3 | C.K2SO4 | D.FeCl3 |
将常温下pH=12的氢氧化钠溶液与pH=2的硫酸溶液分别加热,溶液pH的变化是
| A.前者减小后者不变 | B.前者减小后者增大 | C.都不变 | D.都减小 |
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则( )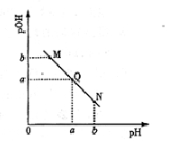
| A.M点所示溶液导电能力强于Q点 |
| B.N点所示溶液中c(CH3COO-)>c(Na+) |
| C.M点和N点所示溶液中水的电离程度相同 |
| D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
室温下,水的电离达到平衡:H2O H+ + OH-。下列叙述正确的是
H+ + OH-。下列叙述正确的是
| A.将水加热,平衡向正反应方向移动,Kw不变 |
| B.向水中加入少量盐酸,平衡向逆反应方向移动,c(H+)增大 |
| C.向水中加入少量NaOH固体,平衡向逆反应方向移动,c(OH-)降低 |
| D.向水中加入少量CH3COONa固体,平衡向正反应方向移动,c(OH-)= c(H+) |
在1 L 1 mol·L-1的氨水中,下列说法正确的是 ( )
| A.含有1 mol NH3分子? | B.含NH3和NH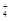 之和为1 mol? 之和为1 mol? |
| C.含NH3·H2O 1 mol? | D.含NH3、NH3·H2O、NH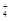 之和为1 mol 之和为1 mol |