题目内容
 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题:(1)A接的是电源的
负
负
极,B是该装置阳
阳
极.(2)写出电解时反应的总离子方程式
2Cu2++2H2O
2Cu+4H++O2↑
| ||
2Cu2++2H2O
2Cu+4H++O2↑
.
| ||
(3)电解后溶液的pH为
1
1
;要使电解后溶液恢复到电解前的状态,则需加入CuO或CuCO3
CuO或CuCO3
,其质量为2g或3.1g
2g或3.1g
.(假设电解前后溶液的体积不变)分析:(1)和电源的负极相连的是电解池的阴极,和电源的正极相连的是电解池的阳极;
(2)电解可溶性的铜盐的实质是电解盐和水,根据电极反应书写电解方程式;
(3)根据电解后所得溶液中氢离子的浓度计算溶液的pH,电解后溶液复原,遵循的原则是:出什么加什么,根据元素守恒来计算所加物质的质量.
(2)电解可溶性的铜盐的实质是电解盐和水,根据电极反应书写电解方程式;
(3)根据电解后所得溶液中氢离子的浓度计算溶液的pH,电解后溶液复原,遵循的原则是:出什么加什么,根据元素守恒来计算所加物质的质量.
解答:解:(1)电解液是蓝色溶液,A电极表面有红色的固态物质生成,所以A极是铜离子得电子,所以A极是阴极,A接的是电源的负极,B电极有无色气体生成,则一定是氢氧根失电子产生的氧气,所以B是该装置阳极,和电源的正极相连,故答案为:负;阳;
(2)阴极反应:2Cu2++4e-→2Cu,阳极反应:4OH-→4e-+2H2O+O2↑,电解时反应的总离子方程式为:2Cu2++2H2O
2Cu+4H++O2↑,故答案为:2Cu2++2H2O
2Cu+4H++O2↑;
(3)取出A电极,洗涤、干燥、称量、电极增重1.6g,所以阴极析出金属铜的质量是1.6g,即0.025mol,所以生成氢离子的物质的量为0.05mol,所以c(H+)=
=0.1mol/L,即pH=1,电解后析出了金属铜和有氧气放出,所以要想溶液复原,需加入 CuO或CuCO3,所加氧化铜的质量=0.025mol×80g/mol=2g,加碳酸铜时则质量=0.025mol×124g/mol=3.1g,故答案为:1;CuO或CuCO3; 2g或3.1g.
(2)阴极反应:2Cu2++4e-→2Cu,阳极反应:4OH-→4e-+2H2O+O2↑,电解时反应的总离子方程式为:2Cu2++2H2O
| ||
| ||
(3)取出A电极,洗涤、干燥、称量、电极增重1.6g,所以阴极析出金属铜的质量是1.6g,即0.025mol,所以生成氢离子的物质的量为0.05mol,所以c(H+)=
| 0.05mol |
| 0.5L |
点评:本题考查学生电解池的工作原理,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
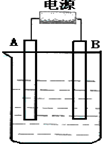 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色硫酸盐溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色硫酸盐溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题: 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题: