题目内容
10.在下列各溶液中,离子一定能大量共存的是( )| A. | 无色溶液中:Na+、Cu2+、Cl- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、CO32-、NH4+ | |
| C. | 能使酚酞试液变红的溶液中:Na+、Cl-、SO42- | |
| D. | 含有大量H+的溶液中:Na+、Cl-、OH- |
分析 A.Cu2+为蓝色;
B.能与金属铝反应放出氢气的溶液,为非氧化性酸或强碱溶液;
C.能使酚酞试液变红的溶液,显碱性;
D.离子之间结合生成水.
解答 解:A.Cu2+为蓝色,与无色不符,故A错误;
B.能与金属铝反应放出氢气的溶液,为非氧化性酸或强碱溶液,酸溶液中不能大量存在CO32-,碱溶液中不能大量存在NH4+,故B错误;
C.能使酚酞试液变红的溶液,显碱性,该组离子之间不反应,可大量共存,故C正确;
D.H+、OH-结合生成水,不能大量共存,故D错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,注意常见离子的颜色,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
5.下列各项中的物质能导电且属于强电解质的是( )
| A. | 氯化钠晶体 | B. | 熔融状态的氯化镁 | ||
| C. | 氨水 | D. | 醋酸 |
15.下列四组实验,根据实验事实得出的结论,正确的是( )
| A. | 在某未知试液中加入浓的NaOH溶液并加热,产生能使湿润的蓝色石蕊试纸变红的气体--原未知试液中一定含有NH4+ | |
| B. | 在某未知试液中加入硝酸银溶液,产生白色沉淀--原未知试液中一定含有Cl- | |
| C. | 用洁净的铂丝蘸取某溶液,置于火焰上灼烧,观察到火焰呈黄色--原溶液中一定含有Na+,不含有K+ | |
| D. | 在某未知试液中滴加过量的稀盐酸得到澄清溶液,再往澄清溶液中加入BaCl2溶液得白色沉淀--原未知试液中一定含有SO42- |
2.如图是实验室制备氯气并进行一系列相关实验的装置(部分夹持设备已省略).
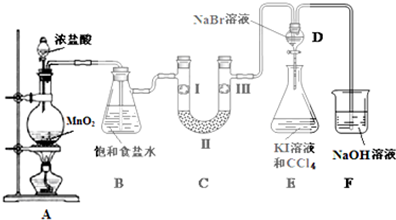
已知:浓硫酸、碱石灰和无水氯化钙均具有吸水性,碱石灰是生石灰和氢氧化钠的混合物.请回答下列问题:
(1)装置A中盛装浓盐酸的仪器名称为分液漏斗,往圆底烧瓶中滴加浓盐酸,反应开始后,圆底烧瓶中发生反应的化学方程式为4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此装置C中Ⅰ、Ⅱ、Ⅲ依次放入d.(填字母)
(4)当向装置D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为橙色,
装置D中发生反应的离子方程式为2Br-+Cl2=Br2+2Cl-.
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是装置E中的溶液分为两层,下层(CCl4层)为紫红色.
(6)装置F中NaOH溶液的作用是吸收多余的氯气,防止污染空气.

已知:浓硫酸、碱石灰和无水氯化钙均具有吸水性,碱石灰是生石灰和氢氧化钠的混合物.请回答下列问题:
(1)装置A中盛装浓盐酸的仪器名称为分液漏斗,往圆底烧瓶中滴加浓盐酸,反应开始后,圆底烧瓶中发生反应的化学方程式为4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此装置C中Ⅰ、Ⅱ、Ⅲ依次放入d.(填字母)
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 浓硫酸 | 碱石灰 | 无水氯化钙 |
| III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
装置D中发生反应的离子方程式为2Br-+Cl2=Br2+2Cl-.
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是装置E中的溶液分为两层,下层(CCl4层)为紫红色.
(6)装置F中NaOH溶液的作用是吸收多余的氯气,防止污染空气.
3.3molH2和3molHe相同的是( )
| A. | 原子数 | B. | 相对分子质量 | C. | 质量 | D. | 质子数 |
