题目内容
在55℃时密闭容器中进行反应:CO(g)+H2O(g)?H2(g)+CO2(g).若CO起始浓度为2mol?L-1,水蒸气的起始浓度为3mol?L-1,达到平衡后,CO2起始浓度为1.2mol?L-1,求CO和H2O(g)的平衡转化率和平衡常数Kc.
考点:用化学平衡常数进行计算
专题:
分析:利用三段式计算平衡时各组分的平衡浓度,
根据转化率=
×100%计算;将平衡浓度代入平衡常数表达式k=
计算.
根据转化率=
| 浓度变化量 |
| 起始浓度 |
| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
解答:
解:CO起始浓度为2mol?L-1,水蒸气的起始浓度为3mol?L-1,达到平衡后,CO2平衡浓度为1.2mol?L-1,则:
CO(g)+H2O(g)?H2(g)+CO2(g)
开始(mol/L):2 3 0 0
变化(mol/L):1.2 1.2 1.2 1.2
平衡(mol/L):0.8 1.8 1.2 1.2
CO的转化率=
×100%=60%,
氢气的转化率=
×100%=40%,
(2)该温度下平衡常数Kc=
=1,
答:CO的转化率为60%,氢气转化率为40%;该温度下,该反应的平衡常数为1.
CO(g)+H2O(g)?H2(g)+CO2(g)
开始(mol/L):2 3 0 0
变化(mol/L):1.2 1.2 1.2 1.2
平衡(mol/L):0.8 1.8 1.2 1.2
CO的转化率=
| 1.2mol/L |
| 2mol/L |
氢气的转化率=
| 1.2mol/L |
| 3mol/L |
(2)该温度下平衡常数Kc=
| 1.2×1.2 |
| 0.8×1.8 |
答:CO的转化率为60%,氢气转化率为40%;该温度下,该反应的平衡常数为1.
点评:本题考查化学平衡的有关计算、平衡常数计算,比较基础,注意三段式解题法的利用.

练习册系列答案
相关题目
下列水溶液一定呈中性的是( )
| A、c(NH4+)=c(Cl-)的NH4Cl溶液 |
| B、c(H+)=1.0×10-7mol?L-1的溶液 |
| C、pH=7的溶液 |
| D、室温下将pH=3的酸与pH=11的碱等体积混合后的溶液 |
类推的思维方式在化学学习与研究中经常采用,但类推出的结论是否正确最终要经过实验的验证.以下类推的结论正确的是( )
| A、由“Cl2+H2O═HCl+HClO”可推出“F2+H2O═HF+HFO” |
| B、HCl的水溶液是强酸,推出HF的水溶液也是强酸 |
| C、由“2Fe+3Cl2═2FeCl3”可推出“2Fe+3I2═2FeI3” |
| D、Na常温下与水剧烈反应,故K常温下也能与水剧烈反应 |
下列说法不正确的是( )
| A、苯和浓硫酸在70~80℃时发生磺化反应 | ||
| B、芳香烃是分子组成符合CnH2n-6(n≥6)的一类物质 | ||
| C、甲苯可以和浓硝酸与浓硫酸的混合物发生硝化反应 | ||
D、等质量的烃(CXHY)耗氧量取决于
|
在下列变化过程中,不涉及化学反应的是( )
| A、金属冶炼 | B、冰雪融化 |
| C、葡萄糖氧化 | D、木柴燃烧 |
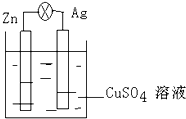 如图所示,在银锌原电池中,以硫酸铜为电解质溶液,锌为
如图所示,在银锌原电池中,以硫酸铜为电解质溶液,锌为