题目内容
10.硒是人体肝脏和肾脏的组成元素之一,现在含有元素硒(Se)的保健品已经进入市场,已知它与氧元素同主族,与K同周期,关于硒的说法中不正确的是( )| A. | 原子序数为34 | B. | 还原性:H2Se<H2S | ||
| C. | 酸性:H2SeO4<HBrO4 | D. | 稳定性:H2Se>AsH3 |
分析 A.Se、O元素同族,与K同周期,其原子序数与O原子序数相差为第二、四周期容纳元素种数;
B.同主族自上而下非金属性减弱,非金属性越强氢化物还原性越弱;
C.同周期自左而右元素非金属性增强,非金属性越强,最高价氧化物对应水化物的酸性增强;
D.同周期自左而右元素非金属性增强,非金属性越强氢化物越稳定.
解答 解:A.Se氧元素同族,与K同周期,其原子序数与O原子序数相差为第二、四周期容纳元素种数,故Se的原子序数=8+8+18=34,故A正确;
B.同主族自上而下非金属性减弱,非金属性越强氢化物还原性越弱,故氢化物还原性H2Se>H2S,故B错误;
C.Se、Br同周期,自左而右元素非金属性增强,非金属性越强,最高价氧化物对应水化物的酸性增强,故酸性酸性:H2SeO4<HBrO4,故C正确;
D.同周期自左而右元素非金属性增强,非金属性越强氢化物越稳定,故氢化物稳定性H2Se>AsH3,故D正确;
故选B.
点评 本题考查元素周期表与元素周期表,注意理解同主族元素性质具有相似性与递变性,理解同主族元素原子序数关系.

练习册系列答案
相关题目
1.下列关系式或离子方程式中,正确的是( )
| A. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+NH3•H2O+2BaSO4↓ | |
| B. | 常温下,0.1 mol•L-1Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| C. | 常温下,将0.1 mol•L-1CH3COOH溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$的值增大到原来的10倍 | |
| D. | 常温下,0.1 mol•L-1HA溶液与0.1 mol•L-1NaOH溶液恰好完全反应时,溶液中一定存在:c(Na+)=c(A-)>c(OH-)=c(H+) |
18.实验室用向上排空气法收集NO2气体,若用150mL的集气瓶收集了一定量的NO2后,将集气瓶倒置于盛满水的水槽里,充分作用后残留60mL气体,将集气瓶从水槽中取出,又见瓶中气体变成红棕色,据此推知收集的NO2气体的体积为(空气按体积比V(N2):V(O2)=4:1计,不考虑N2O4的生成)( )
| A. | 50mL | B. | 72mL | C. | 78mL | D. | 100mL |
5.下列卤代烃能发生消去反应的是( )
| A. | CH3Br | B. | 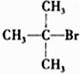 | C. | 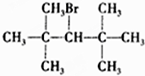 | D. | 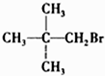 |
15.下列物质中,既含有离子键,又含有共价键的是( )
| A. | Na2O | B. | MgCl2 | C. | NaCl | D. | NaOH |
20.某饱和一元酸跟足量金属钠反应生成0.5gH2.等量的该醇经充分燃烧后生成H2O36g.则该醇应是( )
| A. | 甲醇 | B. | 乙醇 | C. | 丙醇 | D. | 丁醇 |
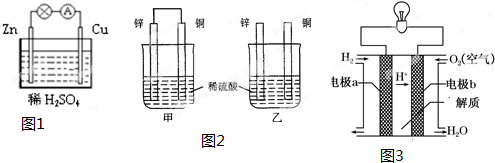
 .
.