题目内容
【题目】下列推断正确的是( )
A. BF3为三角锥形分子
B. NH的电子式为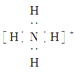 ,离子呈平面正方形结构
,离子呈平面正方形结构
C. CH4分子中的4个C—H键都是氢原子的1s轨道与碳原子的2p轨道形成的s—p σ键
D. CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成C—H σ键
【答案】D
【解析】A,BF3中B的价层电子对数为3+![]() (3-3
(3-3![]() )=3,中心原子B为sp2杂化,BF3为平面三角形分子,A项错误;B,NH4+的电子式为
)=3,中心原子B为sp2杂化,BF3为平面三角形分子,A项错误;B,NH4+的电子式为![]() ,N的价层电子对数为4+
,N的价层电子对数为4+![]() (5-1-4
(5-1-4![]() )=4,中心原子N为sp3杂化,离子呈正四面体形,B项错误;C,CH4中C为sp3杂化,CH4分子中的4个C-H键都是氢原子的1s轨道与4个sp3杂化轨道重叠形成的σ键,C项错误;D,CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成C—H σ键,D项正确;答案选D。
)=4,中心原子N为sp3杂化,离子呈正四面体形,B项错误;C,CH4中C为sp3杂化,CH4分子中的4个C-H键都是氢原子的1s轨道与4个sp3杂化轨道重叠形成的σ键,C项错误;D,CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成C—H σ键,D项正确;答案选D。

练习册系列答案
相关题目