题目内容
10.关于下列各装置图的叙述中,正确的是( )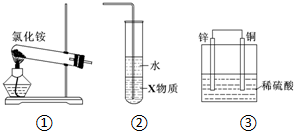
| A. | 实验室用装置①制取氨气 | |
| B. | 装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 | |
| C. | 装置③是电解池,Cu上产生气泡 | |
| D. | 装置③是原电池,锌电极为阴极,发生氧化反应 |
分析 A.氯化铵受热易分解,在管口处HCl与氨气又化合生成氯化铵;
B.为防止倒吸,X物质的密度比水的大,且与水不互溶;
C、装置图可知无电源为原电池;
D.负极发生氧化反应.
解答 解:A.因氯化铵受热易分解,在管口处HCl与氨气又化合生成氯化铵,则不能用装置①制取氨气,故A错误;
B.为防止倒吸,X物质的密度比水的大,且与水不互溶,所以装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸,故B正确;
C、分析装置可知无电源,所以装置是原电池不是电解池,故C错误;
D、装置③是原电池,锌电极失去电子为负极,负极发生氧化反应,故D错误;
故选B.
点评 本题考查实验方案的评价,熟悉气体的制取、防止倒吸的原理、电极反应及物质的性质即可解答,题目难度不大,注意知识积累.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
20.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 78g苯分子中含有的碳碳双键数为3NA | |
| B. | 常温常压下,2g D216O中含中子数、质子数、电子数均为NA | |
| C. | 12g石墨烯(也就是单层石墨)中含有六元环的个数为NA | |
| D. | 7.8g Na2O2含有的阴离子数目为0.2NA |
2.某石油化工产品X的转化关系如图所示,下列判断错误的是( )


| A. | X是制取聚乙烯的单体 | |
| B. | 乙酸→W是酯化反应,也是取代反应 | |
| C. | Y能与钠反应产生氢气 | |
| D. | W能与NaOH溶液反应但不能与硫酸溶液反应 |
19.下列叙述错误的是( )
| A. | 塑料、合成纤维、合成橡胶都是小分子经加聚反应合成 | |
| B. | 石油裂化的主要目的是为了提高轻质液体燃料的产量 | |
| C. | 石油催化重整的目的是为了获得芳香烃 | |
| D. | 重油减压分馏可以降低烃的沸点,使之在较低的温度被蒸出 |
20.某课外小组对一些金属单质和化合物的性质进行研究.
(1)如表为“铝与氯化铜溶液反应”实验报告的一部分:
按反应类型写出实验中发生反应的化学方程式各一个(是离子反应的只写离子方程式)?
置换反应2Al+3CuCl2=3Cu+2AlCl3,
化合反应2Cu+O2+CO2+H2O=Cu2(OH)2CO3.
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡.持续电解,在阴极附近的溶液中还可观察到的现象是有白色沉淀生成,后沉淀逐渐溶解至消失.解释此现象的离子方程式是Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O.
(3)工业上可用铝与软锰矿?主要成分为MnO2?反应来冶炼金属锰.
①用铝与软锰矿冶炼锰的原理是?用化学方程式表示?3MnO2+4Al$\frac{\underline{\;高温\;}}{\;}$3Mn+2Al2O3.
②MnO2在H2O2分解反应中作催化剂.若将适量MnO2加入酸化后的H2O2溶液中,MnO2溶解产生Mn2+,该反应的离子方程式MnO2+H2O2+2H+═Mn2++O2↑+2H2O.
(1)如表为“铝与氯化铜溶液反应”实验报告的一部分:
| 实验报告 | 实验现象 |
| 将打磨过的铝片过量放入一定浓度的CuCl2溶液中 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色. |
| 反应结束后分离出溶液备用 | |
| 红色固体用蒸馏水洗涤后,置于潮湿的空气中 | 一段时间后固体由红色变为绿色(视其主要成分为) |
| Cu2OH2CO3 |
置换反应2Al+3CuCl2=3Cu+2AlCl3,
化合反应2Cu+O2+CO2+H2O=Cu2(OH)2CO3.
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡.持续电解,在阴极附近的溶液中还可观察到的现象是有白色沉淀生成,后沉淀逐渐溶解至消失.解释此现象的离子方程式是Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O.
(3)工业上可用铝与软锰矿?主要成分为MnO2?反应来冶炼金属锰.
①用铝与软锰矿冶炼锰的原理是?用化学方程式表示?3MnO2+4Al$\frac{\underline{\;高温\;}}{\;}$3Mn+2Al2O3.
②MnO2在H2O2分解反应中作催化剂.若将适量MnO2加入酸化后的H2O2溶液中,MnO2溶解产生Mn2+,该反应的离子方程式MnO2+H2O2+2H+═Mn2++O2↑+2H2O.
 乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.结合有关知识,回答下列问题:
乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.结合有关知识,回答下列问题: (1)分子式为C8H10,含有苯环的同分异构体有4种;其中苯环上的一个氢原子被氯原子取代后产生同分异构体数目最少的是
(1)分子式为C8H10,含有苯环的同分异构体有4种;其中苯环上的一个氢原子被氯原子取代后产生同分异构体数目最少的是 ; (填结构简式)
; (填结构简式)