题目内容
20.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )| A. | 78g苯分子中含有的碳碳双键数为3NA | |
| B. | 常温常压下,2g D216O中含中子数、质子数、电子数均为NA | |
| C. | 12g石墨烯(也就是单层石墨)中含有六元环的个数为NA | |
| D. | 7.8g Na2O2含有的阴离子数目为0.2NA |
分析 A.苯分子中不存在碳碳双键;
B.D216O的摩尔质量为20g/mol,其分子中含有质子数、中子数、电子数都是10;
C.石墨中,每个碳原子为3个六元环共用,利用均摊法计算出12gC含有的六元环数目;
D.过氧化钠中的阴离子为过氧根离子,7.8g过氧化钠的物质的量为0.1mol,含有0.1mol过氧根离子.
解答 解:A.苯分子中的碳碳键为一种具有单键和双键之间的独特键,不存在碳碳双键,故A错误;
B.2gD216O的物质的量为:$\frac{2}{20g/mol}$=0.1mol,0.1molD216O中含有质子、中子和电子的物质的量都是1mol,含中子数、质子数、电子数均为NA,故B正确;
C.12g石墨中含有碳的物质的量为:$\frac{12g}{12g/mol}$=1mol,石墨中,每个碳为3个六元环共用,则每个六元环中含有的碳原子数为:$\frac{1}{3}$×6=2,即:每一个六元环中含有2个C,所以1molC写出的六元环为:$\frac{1mol}{2}$=0.5mol,含有六元环的个数为0.5NA,故C错误;
D.7.8g过氧化钠的物质的量为:$\frac{7.8g}{78g/mol}$=0.1mol,0.1mol过氧化钠中含有0.1mol过氧根离子,含有的阴离子数目为0.1NA,故D错误;
故选B.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意熟练掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;C为易错点,注意把握均摊法的应用.

练习册系列答案
相关题目
10.下列物质不能发生水解反应的是( )
| A. | 葡萄糖 | B. | 淀粉 | C. | 油脂 | D. | 蛋白质 |
11.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,22.4LC2H2含σ键3NA,π键2NA | |
| B. | 在含4molSi-O键的二氧化硅中,氧原子数为4NA | |
| C. | 1.8gH218O中含有的中子数为NA | |
| D. | 标准状况下,7.1g氯气与足量石灰乳充分反应转移电子数为0.1NA |
8.下列装置或操作能达到实验目的是( )
| A. | 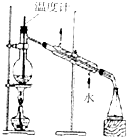 石油的分馏 | B. | 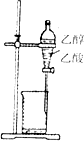 除去乙醇中的乙酸 | ||
| C. | 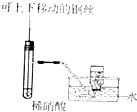 制备并收集少量NO | D. | 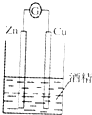 形成原电池 |
5.除去括号内杂质所用试剂和方法,正确的是( )
| A. | 乙醇(乙酸) 生石灰 过滤 | |
| B. | 溴乙烷(乙醇) 水 分液 | |
| C. | 乙醇(苯酚) NaOH溶液 分液 | |
| D. | 苯甲酸(苯甲酸钠) 硫酸 蒸馏 |
12.为证明溴乙烷在NaOH的乙醇溶液中加热发生消去反应,可将反应后的气体通入( )
| A. | 溴水 | B. | AgNO3溶液 | C. | 酸性KMnO4溶液 | D. | 酸化的AgNO3溶液 |
9.下列物质的说法不正确的是( )
| A. | 液化石油气是通过石油催化裂化或裂解得到的 | |
| B. | 芳香烃主要来自于煤的干馏后的煤焦油 | |
| C. | 汽油、煤油、柴油主要来自于石油的常压蒸馏 | |
| D. | 乙烯是石油裂解后的产物 |
10.关于下列各装置图的叙述中,正确的是( )
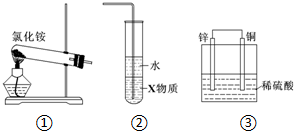

| A. | 实验室用装置①制取氨气 | |
| B. | 装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 | |
| C. | 装置③是电解池,Cu上产生气泡 | |
| D. | 装置③是原电池,锌电极为阴极,发生氧化反应 |