��Ŀ����
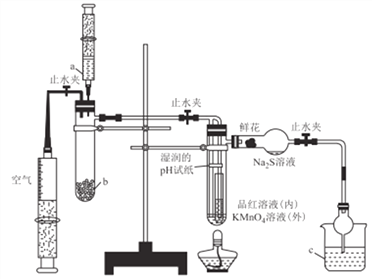
����Ŀ��ij�ֻ���ز�����ʯīϩ��أ��ɳ��5���ӣ�ͨ��2Сʱ��һ��ʯīϩ�����(2Li+S8=Li2S8)����ԭ��ʾ��ͼ��ͼ�������йظõ��˵������ȷ����
A. ����������н����б�������ߵĵ缫����
B. ���ʱA�缫Ϊ������������ԭ��Ӧ
C. ���ʱB�缫�ķ�Ӧ:Li2S8-2e-=2Li++S8
D. �ֻ�ʹ��ʱ���Ӵ�A�缫�����ֻ���·������B�缫���پ�����ص��������A�缫
���𰸡�D
��������A����λ�����ĵ缫����ʧȥ���ӵ����ʵ���Խ�࣬��õ��ĵ���Խ�࣬����Խ�ߣ�Li�����н���Ԫ����ԭ������С�Ľ��������Խ���������н����б�������ߵĵ缫���ϣ���A��ȷ��B��ԭ������������������ƶ�����ͼ��֪������Դʱ��BΪ������AΪ��������������ʧ���ӵ�������Ӧ�������������ʱ����Ϊ������������ԭ��Ӧ����B��ȷ��C��B�缫��S8�õ�������Li2S8����B�缫�ķ�Ӧ��2Li++S8+2e-�TLi2S8����C��ȷ��D������ֻ���ڵ缫�͵������ƶ������Ӳ����ڵ������Һ���ƶ�����D����ѡD��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��NH3��Ϊһ����Ҫ����ԭ�ϣ�������Ӧ���ڹ�ҵ�����������й����ʷ�Ӧ�Ĵ����о������������863 �ƻ���
(1)���������н�ǿ��ѡ���ԡ���֪:
��ӦI:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ��H1=-905kJ��mol-1
4NO(g)+6H2O(g) ��H1=-905kJ��mol-1
��ӦII:4NH3(g)+3O2(g) ![]() 2N2(g)+6H2O(g) ��H2=-1266.6kJ��mol-1
2N2(g)+6H2O(g) ��H2=-1266.6kJ��mol-1
д��NO �ֽ�����N2��O2���Ȼ�ѧ����ʽ______________________________________��
(2)N2OҲ�ɷֽ�����N2��O2�����ĸ������ܱ������а����±���Ӧ���������壬����2N2O(g)![]() 2N2(g)+O2(g)������I��II��III��N2Oƽ��ת��������ͼ��ʾ��
2N2(g)+O2(g)������I��II��III��N2Oƽ��ת��������ͼ��ʾ��
���� | �ݻ�/L | ��ʼ���ʵ���/mol | ||
N2O | N2 | O2 | ||
I | V1 | 0.1 | 0 | 0 |
II | 1.0 | 0.1 | 0 | 0 |
III | V2 | 0.1 | 0 | 0 |
IV | 1.0 | 0.06 | 0.06 | 0.04 |
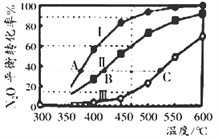
�ٸ÷�Ӧ�ġ�H_________0(�>������=������<��);
��ͼ��A��B��C ���㴦�����ڵ���ѹǿ���ɴ�С��˳����_____________________��
������IV��470����з�Ӧʱ����ʼ����:v(N2O)��____v (N2O)��(�>������=������<��)��
(3)��������ʱ�ᷢ����������������ӦI��II��Ϊ����ij�����Ը÷�Ӧ��ѡ���ԣ���20L�ܱ������г�lmolNH3��2molO2�����һ��ʱ�����й����ʵ�����ϵ��ͼ:
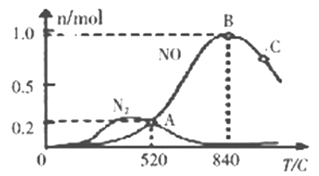
�ٸô����ڵ���ʱѡ��Ӧ________(�I����II��)��
��C���B����������NO�����ʵ����ٵ�ԭ�������_________________________________��