题目内容
【题目】下列条件的改变,一定会同时影响化学反应速率和化学平衡的是
A. 浓度 B. 压强 C. 温度 D. 催化剂
【答案】C
【解析】A、增大固体和纯液体的量,浓度为常数,对反应速率和化学平衡无影响,选项A错误;B、在化学反应前后体积不变的情况下,改变压强对化学平衡无影响,选项B错误;C、所有化学反应都反应热,温度对于任何反应的反应速率和化学平衡都有影响,选项C正确;D、催化剂能改变反应速率,不能使化学平衡移动,选项D错误。答案选C。

练习册系列答案
相关题目
【题目】
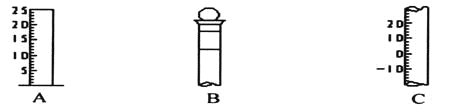
(1)请写出下列仪器的名称:A ,B ,C 。
(2)仪器B上标记有 (填序号)。
①质量 ②温度 ③刻度线 ④浓度 ⑤容积
Ⅱ.现用98%的浓H2SO4(密度为1.84g/cm3)来配制480mL0.2mol/L的稀H2SO4。
有关操作为:①计算所需浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释、冷却 ④转移、洗涤 ⑤定容 ⑥摇匀。回答下列问题
(3)应用量筒量取的浓硫酸体积是 mL,实验中所用的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还有 。
(4)第③步中稀释浓硫酸的操作是 。
(5)将所配制的稀H2SO4进行测定,发现实际浓度大于0.2mol/L。请你分析下列哪些操作会引起所配浓度偏大(填写字母) 。
A.用量筒量取浓硫酸时,仰视量筒的刻度 |
B.容量瓶未干燥即用来配制溶液 |
C.浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容 |
D.往容量瓶转移时,有少量液体溅出 |
E.烧杯未进行洗涤
F.在容量瓶中定容时俯视容量瓶刻度线
G.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。