题目内容
【题目】碳、氮、硫的化合物在生产生活中广泛存在。请回答:
(1)以CO2与NH3为原料可合成化肥尿素[CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-l59.5kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l) ΔH=-160.5kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式__。
(2)T温度时在容积为2L的恒容密闭容器中只充入1.00molNO2气体发生反应:2NO(g)+O2(g)![]() 2NO2(g) H<0。不同时刻测得容器中n(NO2)如下表:
2NO2(g) H<0。不同时刻测得容器中n(NO2)如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
①升高温度K值___(增大、减小),T温度时化学平衡常数K=___mol-1·L
②从0~2s该反应的平均速率v(NO2)=___。
③对可逆反应2NO(g)+O2(g)![]() 2NO2(g) H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是___。
2NO2(g) H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是___。
A.混合气体的密度不再变化
B.混合气体的压强不再变化
C.氧气的转化率不再变化
D.N2、O2、NO的物质的量之比为1:1:2
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等。
①已知Na2SO3水溶液显碱性,原因是___(写出主要反应的离子方程式),该溶液中,c(Na+)___2c(SO32-)+c(HSO3-)(填“>”“<”或“=”)。
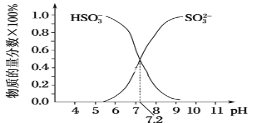
②在某NaHSO3、Na2SO3混合溶液中HSO3-、SO32-物质的量分数随pH变化曲线如图所示(部分),根据图示,则SO32-的第一步水解平衡常数=____。
【答案】2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) △H=-320.0kJ/mol 减小 8 0.0875mol/(L·s) BC SO32-+H2O![]() HSO3-+OH- > 10-6.8
HSO3-+OH- > 10-6.8
【解析】
(1)依据热化学方程式和盖斯定律计算①+②得到CO2与NH3合成尿素和液态水的热化学反应方程式;
(2)①2NO(g)+O2(g)![]() 2NO2(g) H<0,温度升高,平衡逆向移动,则K减小;
2NO2(g) H<0,温度升高,平衡逆向移动,则K减小;  ,根据化学平衡常数K1=
,根据化学平衡常数K1=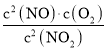 计算K1,进而计算2NO(g)+O2(g)2NO2(g)化学平衡常数K=
计算K1,进而计算2NO(g)+O2(g)2NO2(g)化学平衡常数K=![]() ;
;
②根据v=![]() 计算出前2s内v(NO2);
计算出前2s内v(NO2);
③根据化学平衡状态分析;
(3)①亚硫酸根离子水解导致溶液显示碱性,根据电荷守恒确定离子浓度的关系;
②根据水解平衡常数表达式结合图中数据来计算。
(1)①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-l59.5kJmol-1,②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l)△H=-160.5kJmol-1,依据热化学方程式和盖斯定律计算①+②得到CO2与NH3合成尿素和液态水的热化学反应方程式为2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) △H=-320.0kJ/mol,故答案为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) △H=-320.0kJ/mol;
(2)①2NO(g)+O2(g)![]() 2NO2(g) H<0,温度升高,平衡逆向移动,则K减小;
2NO2(g) H<0,温度升高,平衡逆向移动,则K减小;  ,根据化学平衡常数K1=
,根据化学平衡常数K1=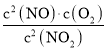 =0.125,所以2NO(g)+O2(g)2NO2(g)化学平衡常数K=
=0.125,所以2NO(g)+O2(g)2NO2(g)化学平衡常数K=![]() =8,故答案为:减小;8;
=8,故答案为:减小;8;
②根据表中数据计算出前2s内v(NO2)=![]() =
=![]() =
=![]() =0.0875mol/(Ls),故答案为:0.0875mol/(L·s);
=0.0875mol/(Ls),故答案为:0.0875mol/(L·s);
③A.该可逆反应在恒容条件下进行,质量反应前后不变,则混合气体的密度始终不变化,错误;
B.该可逆反应在恒容条件下进行,正向进行,体积减小,则压强减小,当混合气体的压强不再变化时,该反应达到化学平衡状态,正确;
C.反应没平衡时,氧气的转化率会变化,当氧气的转化率不变化时,该反应达到化学平衡状态,正确;
D.物质的量之比不能作为判断化学平衡状态依据,错误;
综上,正确的为BC,故答案为:BC;
(3)①亚硫酸根离子水解导致溶液显示碱性,原理是:SO32-+H2OHSO3-+OH-,所以,该溶液中,c(H
②亚硫酸根离子的水解平衡常数K= 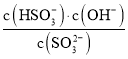 ,当pH=7.2时,SO32-、HSO3-浓度相等,所以K=c(OH-)=10-6.8,故答案为:10-6.8。
,当pH=7.2时,SO32-、HSO3-浓度相等,所以K=c(OH-)=10-6.8,故答案为:10-6.8。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案