��Ŀ����
����Ŀ��һ������CO2��������̼������ɱ�ĺ�ѹ�ܱ������з�ӦC��s��+CO2��g��![]() 2CO��g����ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ��ͼ��ʾ��
2CO��g����ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ��ͼ��ʾ��
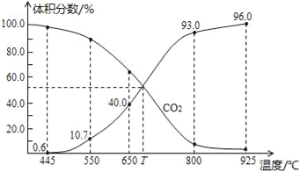
��֪�����ѹ��P�֣�=������ѹ��P�ܣ����������������˵������ȷ����
A.550��ʱ��������������壬v����v������С��ƽ�ⲻ�ƶ�
B.650��ʱ����Ӧ��ƽ���CO2��ת����Ϊ25.0%
C.T��ʱ��������������CO2��CO��ƽ�����ƶ�
D.925��ʱ����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=23.04P��
���𰸡�A
��������
��ѹ�ܱ������з�ӦC��s��+CO2��g��![]() 2CO��g������Ӧ������������������¶����ߣ�������̼����������½�����Ӧ�����ƶ����ʷ�ӦΪ���ȷ�Ӧ��
2CO��g������Ӧ������������������¶����ߣ�������̼����������½�����Ӧ�����ƶ����ʷ�ӦΪ���ȷ�Ӧ��
A. 550��ʱ��������������壬�����������ͬ�ں��ݻ����¼�Сѹǿ��v����v������С��ƽ�������ƶ���A����
B. ��ͼ��֪��650��ʱ����Ӧ��ƽ���һ����̼���������Ϊ40%���迪ʼ����Ķ�����̼Ϊ1mol��ת���� xmol����ƽ��ʱһ����̼��Ϊ2xmol��������̼Ϊ (1-x)mol��![]() ��x=0.25mol����CO2��ת����Ϊ25.0%��B��ȷ��
��x=0.25mol����CO2��ת����Ϊ25.0%��B��ȷ��
C. ��ͼ��֪��T��ʱ���ﵽƽ��״̬ʱ���������������Ϊ50%��������������CO2��CO��ƽ�ⲻ�ƶ���C����
D. 925��ʱ��һ����̼���������Ϊ96%���������̼���������Ϊ4%����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��![]() ����D��ȷ��
����D��ȷ��
��ΪA��

 ����ѧУ�ֲ����ܲ�ϵ�д�
����ѧУ�ֲ����ܲ�ϵ�д� �ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
�ƸԺ���ȫ�����Ų��Ծ�ϵ�д�����Ŀ�������£���һԪ��HA����Һ��KOH��Һ�������ϣ���������仯����ʵ���������±���
ʵ���� | ��ʼŨ��/(mol��L-1) | ��Ӧ����Һ��pH | |
c(HA) | c(KOH) | ||
�� | 0.1 | 0.1 | 9 |
�� | x | 0.2 | 7 |
��1��ʵ��ٷ�Ӧ�����ҺpH=9��ԭ����___�������ӷ���ʽ��ʾ����
��2��ʵ��ٺ�ʵ�����ˮ�ĵ���̶Ƚϴ����__������Һ����ˮ�������c(OH-)=__��
��3��x__0.2(������������������=��)����x=a����������HA�ĵ���ƽ�ⳣ��Ka=__���ú�a�ı���ʽ��ʾ����
��4��������֪Ũ�ȵ�KOH�ζ�δ֪Ũ�ȵ�һԪ��HA���ζ��յ���жϷ�����__��
����Ŀ�������������������������������Ҫ�����á��ش��������⣺
(1)��֪4NH3(g)+5O2(g)=4NO(g)+6H2O(g)��H1=��alkJ/mol��4NH3(g)+6NO(g)=5N2(g)+6H2O(g)��H2=��bkJ/mol��H2O(1)=H2O(g)��H3=+ckJ/mol��д����298Kʱ������ȼ������N2���Ȼ�ѧ����ʽ___________��
(2)�����еļ��쵰��(Mb)����O2�������MbO2��Mb(aq)+O2(g)![]() MbO2(aq)������k����k���ֱ��ʾ����Ӧ���淴Ӧ�����ʳ�������V��=k����c(Mb)��P(O2)��V��=k����c(MbO2)��37��ʱ��ü��쵰�Ľ�϶�(��)��P(O2)�Ĺ�ϵ���±�[��϶�(��)ָ����O2��ϵļ��쵰��ռ�ܼ��쵰�İٷֱ�]��
MbO2(aq)������k����k���ֱ��ʾ����Ӧ���淴Ӧ�����ʳ�������V��=k����c(Mb)��P(O2)��V��=k����c(MbO2)��37��ʱ��ü��쵰�Ľ�϶�(��)��P(O2)�Ĺ�ϵ���±�[��϶�(��)ָ����O2��ϵļ��쵰��ռ�ܼ��쵰�İٷֱ�]��
P(O2) | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
����MbO2%�� | 50.0 | 67.0 | 80.0 | 85.0 | 88.0 | 90.3 | 91.0 |
�ټ���37�桢P(O2)Ϊ2.00kPaʱ��������Ӧ��ƽ�ⳣ��K=___________��
�ڵ���ƽ��ʱ���쵰����O2�Ľ�϶�(��)��O2��ѹǿ[P(O2)]֮��Ĺ�ϵʽ��=___________(�ú���k����k����ʽ�ӱ�ʾ)��
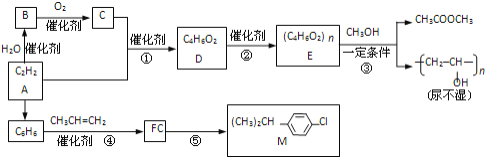
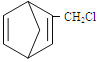
(3)���ɼ��쵰�ĸʰ���(NH2CH2COOH)��һ���������ʣ�����Һ��������������ʽ���ڣ���ת����ϵ���£�
![]()
![]()
![]()
![]()
![]()
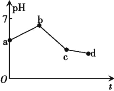
�ڸʰ�����Һ�м�������������ӵİٷֺ������Ĺ�ϵ��ͼ��ʾ��
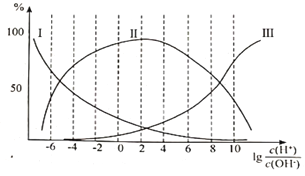
�ٴ��ʰ�����Һ��___________�ԣ�����Һ������ʱ�������ӵ�Ũ���ɴ�С��˳��Ϊ___________��
����![]() =8����Һ�м������HClʱ����Ӧ�����ӷ���ʽΪ___________��
=8����Һ�м������HClʱ����Ӧ�����ӷ���ʽΪ___________��
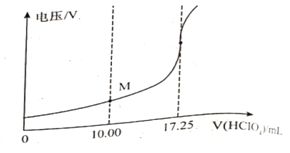
���õ�λ�ζ����ɲⶨij�ʰ�����Ʒ�Ĵ���.
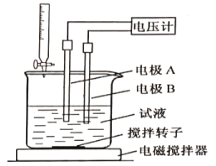
��ȡ��Ʒ150mg����һ�������£���0.1000mol/L�ĸ�������Һ�ζ�(��ʰ���1�U1������Ӧ)����õ�ѹ�仯�����HClO4��Һ�������ϵ����ͼ�����հ���ʵ�飬����HClO4��Һ�����Ϊ0.25mL������Ʒ�Ĵ���Ϊ___________%(����������һλС��)