题目内容
【题目】咖啡酸具有止血、镇咳、祛痰等疗效,其结构简式为![]() ,下列有关咖啡酸的说法中,不正确的是( )
,下列有关咖啡酸的说法中,不正确的是( )
A.咖啡酸遇FeCl3溶液显紫色
B.咖啡酸可以发生加成、酯化、加聚等反应
C.1mol咖啡酸最多能与3molNaOH发生反应
D.1mol咖啡酸与饱和溴水反应,最多消耗2molBr2
【答案】D
【解析】
A.咖啡酸含有酚羟基,酚羟基遇到FeCl3溶液显紫色,故A正确;
B.咖啡酸分子中含有酚羟基、C=C以及-COOH,可以发生加成、酯化、加聚等反应,故B正确;
C. 酚羟基和羧基能和氢氧化钠反应,所以1mol咖啡酸与NaOH溶液反应最多消耗3mol的NaOH,故C正确;
D.咖啡酸分子中含有2个酚羟基,且临位或对位上有3个H可被取代,含有C=C,可发生加成反应,则1mol咖啡酸与饱和溴水反应,最多消耗4molBr2,故D错误;
故答案选D。

【题目】工业废气和汽车尾气含有多种氮氧化物,以NOx表示,NOx能破坏臭氧层,产生光化学烟雾,是造成大气污染的来源之一。按要求回答下列问题:
(1)NO2与N2O4存在以下转化关系:2NO2(g)![]() N2O4(g)。
N2O4(g)。
①已知:标准状况(25℃、101kPa)下,由最稳定的单质生成1mol化合物的焓变(或反应热),称为该化合物的标准摩尔生成焓。几种氧化物的标准摩尔生成焓如表所示:
物质 | NO(g) | NO2(g) | N2O4(g) | CO(g) |
标准摩尔生成焓/(kJ·mol-1) | 90.25 | 33.18 | 9.16 | -110.53 |
则NO2转化成N2O4的热化学方程式为__。
②将一定量N2O4投入固定容积的恒温容器中,下述现象能说明反应达到平衡状态的是__(填标号)。
A.v(N2O4)=2v(NO2) B.气体的密度不变
C.![]() 不变 D.气体的平均相对分子质量不变
不变 D.气体的平均相对分子质量不变
③达到平衡后,保持温度不变,将气体体积压缩到原来的一半,再次达到平衡时,混合气体颜色____填“变深”“变浅”或“不变”),判断理由是___。
(2)在容积均为2L的甲、乙两个恒容密闭容器中,分别充入等量NO2,发生反应:2NO2(g)![]() 2NO(g)+O2(g)。保持温度分别为T1、T2,测得
2NO(g)+O2(g)。保持温度分别为T1、T2,测得![]() n(NO2)与n(O2)随时间的变化如图所示:
n(NO2)与n(O2)随时间的变化如图所示:
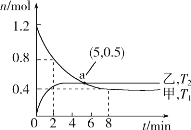
①T1时,反应从开始到第2min,平均速率v(O2)=__,该温度下平衡常数K=__。
②实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响,下列有关说法正确的是__(填标号)。
A.反应正向放热
B.a点处,v逆(甲)<v逆(乙)
C.k正(T2)>k正(T1)
D.温度改变,k正与k逆的比值不变
(3)硫代硫酸钠(Na2S2O3)在碱性溶液中是较强的还原剂,可用于净化氧化度较高的NOx废气,使之转化为无毒、无污染的N2。请写出NO2与硫代硫酸钠碱性溶液反应的离子方程式:__。