题目内容
在下图中,横坐标为某溶液中加入溶质的物质的量,纵坐标为生成沉淀的量:
从A~D中选择符合表中各项要求填入相应位置。
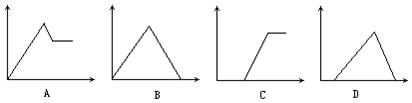
从A~D中选择符合表中各项要求填入相应位置。

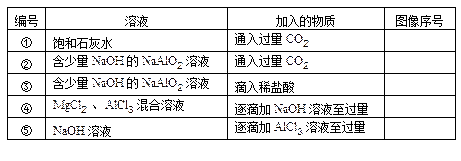
BCDAC</PGN0098B.TXT/PGN>
①饱和石灰水中通入二氧化碳,立即生成沉淀,当通入过量二氧化碳时,沉淀逐渐溶解,当通入二氧化碳跟原溶液中氢氧化钙的物质的量比为2∶1时,沉淀完全溶解,反应的化学方程式是:
Ca(OH)2+CO2====CaCO3↓+H2O
CaCO3+CO2+H2O====Ca(HCO3)2
②二氧化碳通入含氢氧化钠的偏铝酸钠溶液中,首先跟氢氧化钠反应,没有沉淀生成:
2NaOH+CO2====Na2CO3+H2O
把氢氧化钠都中和完以后,接着二氧化碳跟偏铝酸钠反应:
NaAlO2+CO2+2H2O====Al(OH)3↓+NaHCO3
当偏铝酸钠反应完以后,再通入二氧化碳,沉淀不再增加,但是也不会溶解。
③稀盐酸加到含氢氧化钠的偏铝酸钠溶液中时,首先中和氢氧化钠,没有沉淀生成:
NaOH+HCl====NaCl+H2O
然后盐酸跟偏铝酸钠反应,生成沉淀,加入过量的盐酸时,生成的氢氧化铝沉淀又溶解于盐酸中:
NaAlO2+HCl+H2O====Al(OH)3↓+NaCl
Al(OH)3+3HCl====AlCl3+3H2O
④氢氧化钠逐滴加到氯化镁和氯化铝的混合溶液中,观察到有白色沉淀生成,沉淀逐渐增加:
MgCl2+2NaOH====Mg(OH)2↓+2NaCl
AlCl3+3NaOH====Al(OH)3↓+3NaCl
当溶液中的Mg2+、Al3+都用完时,沉淀量最大,再加过量的氢氧化钠溶液,沉淀开始减少,到氢氧化铝全部溶解时,沉淀的量不再减少:
Al(OH)3+NaOH====NaAlO2+2H2O
⑤三氯化铝溶液逐滴加氢氧化钠溶液时,先观察到有白色沉淀,由于氢氧化钠过量,振荡,沉淀溶解,直至氢氧化钠消耗尽:
AlCl3+3NaOH====Al(OH)3↓+3NaCl
Al(OH)3+NaOH====NaAlO2+2H2O
继续滴加三氯化铝,有白色沉淀生成,沉淀量不断增加,当溶液中AlO2-离子消耗尽以后,再加三氯化铝,沉淀的量不变。
3NaAlO2+AlCl3+6H2O====4Al(OH)3↓
Ca(OH)2+CO2====CaCO3↓+H2O
CaCO3+CO2+H2O====Ca(HCO3)2
②二氧化碳通入含氢氧化钠的偏铝酸钠溶液中,首先跟氢氧化钠反应,没有沉淀生成:
2NaOH+CO2====Na2CO3+H2O
把氢氧化钠都中和完以后,接着二氧化碳跟偏铝酸钠反应:
NaAlO2+CO2+2H2O====Al(OH)3↓+NaHCO3
当偏铝酸钠反应完以后,再通入二氧化碳,沉淀不再增加,但是也不会溶解。
③稀盐酸加到含氢氧化钠的偏铝酸钠溶液中时,首先中和氢氧化钠,没有沉淀生成:
NaOH+HCl====NaCl+H2O
然后盐酸跟偏铝酸钠反应,生成沉淀,加入过量的盐酸时,生成的氢氧化铝沉淀又溶解于盐酸中:
NaAlO2+HCl+H2O====Al(OH)3↓+NaCl
Al(OH)3+3HCl====AlCl3+3H2O
④氢氧化钠逐滴加到氯化镁和氯化铝的混合溶液中,观察到有白色沉淀生成,沉淀逐渐增加:
MgCl2+2NaOH====Mg(OH)2↓+2NaCl
AlCl3+3NaOH====Al(OH)3↓+3NaCl
当溶液中的Mg2+、Al3+都用完时,沉淀量最大,再加过量的氢氧化钠溶液,沉淀开始减少,到氢氧化铝全部溶解时,沉淀的量不再减少:
Al(OH)3+NaOH====NaAlO2+2H2O
⑤三氯化铝溶液逐滴加氢氧化钠溶液时,先观察到有白色沉淀,由于氢氧化钠过量,振荡,沉淀溶解,直至氢氧化钠消耗尽:
AlCl3+3NaOH====Al(OH)3↓+3NaCl
Al(OH)3+NaOH====NaAlO2+2H2O
继续滴加三氯化铝,有白色沉淀生成,沉淀量不断增加,当溶液中AlO2-离子消耗尽以后,再加三氯化铝,沉淀的量不变。
3NaAlO2+AlCl3+6H2O====4Al(OH)3↓

练习册系列答案
相关题目
 和H2F
和H2F