题目内容
20.W、X、Y、Z、R为五种短周期主族非金属元素,它们在元素周期表中的相对位置如图所示.下列关于五种元素的说法正确的是( )| W | X | R | |
| Y | Z |
| A. | 粒子半径:原子半径最大的是W,简单阴离子半径最小的是R | |
| B. | 单质:氧化性最强的是Z,还原性最强的是Y | |
| C. | 最高价氧化物对应水化物:酸性最强的是Z,水溶性最差的是Y | |
| D. | 最简单氢化物:沸点最高的是X,稳定性最差的是W |
分析 W、X、Y、Z、R为五种短周期主族非金属元素,依据它们在元素周期表中的相对位置可以判断得出W为氮,X为氧,Y为硅,Z为氯,R为氟,据此解答即可.
解答 解:W、X、Y、Z、R为五种短周期主族非金属元素,那么W应为N元素,若为C元素,Y即为Al,不符合题意,故据此推断得出W为氮,X为氧,Y为硅,Z为氯,R为氟,
A、电子层数越多,原子半径越大,电子层数一样多,原子序数越小,半径越大,故原子半径最大的是Al,简单阴离子半径最小的也是Al3+,故A错误;
B、元素的非金属性越强,其单质氧化性越强,因为非金属性R>Z,故非金属性最强的是F,还原性最强的是Al,故B错误;
C、元素的非金属性越强,其最高价氧化物的水化物酸性越强,由于F无正价,故酸性最强的是高氯酸,硅酸是难溶于水的酸,故C正确;
D、由于水中存在氢键,故水的沸点最高,元素的非金属性越强,其氢化物越稳定,所以简单氢化物的稳定性最差的是SiH4,故D错误,
故选C.
点评 本题主要考查元素周期表与元素周期律,难度不大,侧重对元素周期律的考查,注意整体把握元素周期表的结构.

练习册系列答案
相关题目
18.混合下列各组物质使之充分反应,将所得混合物加热蒸干,并在300℃灼烧至质量不变为止,最终残留固体为纯净物的是( )
| A. | 向CuSO4溶液中加入适量铁粉 | B. | 等浓度等体积的(NH4)2SO4和BaCl2 | ||
| C. | 等物质的量的NaHCO3和Na2O2 | D. | 在NaBr溶液中通入过量的Cl2 |
15.下列四组物质,组内每种混合物都能用分液漏斗分离的是( )
| A. | 乙酸乙酯和水、酒精和水、植物油和水 | |
| B. | 四氯化碳和水、溴苯和水、硝基苯和水 | |
| C. | 甘油和水、乙酸和乙醇、乙酸和水 | |
| D. | 水和植物油、己烷和水、苯和水 |
5.已知反应A2(g)+2B2(g)?2AB2(g)△H<0,下列说法正确的( )
| A. | 升高温度,正向反应速率增加,逆向反应速率减小 | |
| B. | 升高温度有利于反应速率增加,从而缩短达到平衡的时间 | |
| C. | 若反应在密闭体系内进行,通入He气,体系压强增大,反应速率增大 | |
| D. | 若反应在恒压体系内进行,通往He气,体系压强不变,反应速率不变 |
12.食品香精菠萝酯的生产路线(反应条件略去)如下,下列叙述错误的是( )
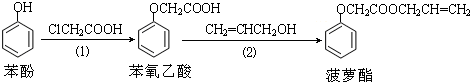
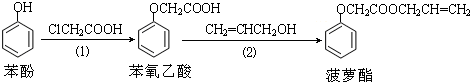
| A. | 步骤(1)产物中残留的苯酚可用FeCl3溶液检验 | |
| B. | 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应 | |
| C. | 苯酚和菠萝酯均可与溴水发生反应 | |
| D. | 步骤(2)产物中残留的烯丙醇可用溴水检验 |
9.已知下表均为烷烃分子的化学式,且它们的一氯取代物只有一种
则第6项烷烃分子的化学式( )
| 1 | 2 | 3 | 4 | 5 | 6 | … |
| … | C2H6 | C5H12 | C8H18 | … | … | … |
| A. | C16H34 | B. | C17H36 | C. | C26H54 | D. | C27H56 |
10.甲、乙、丙都是短周期元素,其中甲、乙两元素原子的最外层电子数分别是次外层电子数的2倍和3倍,丙元素原子K层和M层电子数之积与L层的电子数相同.则下列判断不正确的是( )
| A. | 乙元素的族序数比甲元素的族序数大 | |
| B. | 甲、丙元素最高价氧化物对应水化物的酸性强弱顺序:甲>丙 | |
| C. | 原子半径由大到小的顺序:丙>甲>乙 | |
| D. | 含乙元素的化合物数目比含甲或丙元素的化合物数目多 |
 甲烷、甲醇、CO、H2、CO2均是重要的化工原料.
甲烷、甲醇、CO、H2、CO2均是重要的化工原料.