题目内容
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
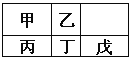
A. 原子半径:丙<丁<戊
B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊
D. 最外层电子数:甲>乙
【答案】C
【解析】试题分析:A、丙、丁、戊在周期表中同一周期,原子半径从左到右逐渐减小,则有丙>丁>戊,故A错误;B、甲、丙在同一主族,同主族元素从上到下元素的金属性逐渐增强,故甲<丙,故B错误;C、丙、丁、戊在周期表中同一周期,同一周期元素的金属性从左到右之间减弱,对应的最高价氧化物的水化物的碱性逐渐减弱,则有氢氧化物碱性:丙>丁>戊,故C正确;D、甲、乙在同一周期,同一周期元素的原子序数逐渐增大,最外层电子数逐渐增多,则有甲<乙,故D错误;故选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】下表是元素周期表的前三周期:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0[ | |
一 | A | |||||||
二 | B | C | D | E | F | |||
三[ | G | H | I | J |
回答下列问题:
(1)J元素的元素的名称:___________。
(2)G元素与I 元素形成的化合物的电子式是___________,
A、G、E形成的化合物中含有的化学键类型为_____________________________。
(3)表格中十种元素的最高氧化物对应的水化物中,酸性最强的是_____________,
属于两性氢氧化物的是_______________(用化合物的化学式表示)。
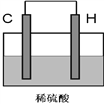
(4)将H单质与C的一种单质(导体)按如下图装置连接,其中C极为_________极(填正或负),并写出该电极反应式为:____________________。