籾朕坪否
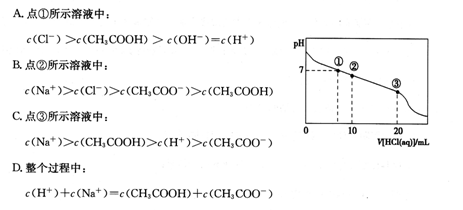
壓25≧扮繍pH﹆11 議NaOH 卑匣嚥pH﹆3 議CH3COOH卑甸吉悶持詞栽朔⇧和双購狼塀嶄屎鳩議頁
| A⤴c (Na+)=c(CH3COO⇩)+c(CH3COOH) |
| B⤴c(H+)=c(CH3COO⇩)+c(OH匯) |
| C⤴c (Na+) > c (CH3COO⇩)>c(OH⇩)>c(H+) |
| D⤴c (CH3COO⇩)>c(Na+)>c(H+)>c(OH⇩) |
D
盾裂編籾蛍裂⦿25≧扮pH﹆11 議NaOH 卑匣⇧c(OH⇩)=10-3mol/L; pH﹆3 議CH3COOH卑甸c(H+)=10-3mol/L.喇噐NaOH頁膿珠⇧頼畠窮宣⇧遇閑磨頁樋磨⇧何蛍窮宣。咀緩c(CH3COOH)>c(NaOH)。功象麗創便冴c (Na+)<c(CH3COO⇩)+c(CH3COOH)。A危列。壓乎卑匣嶄CH3COOH窮宣恢伏議H+瓜NaOH嶄才匯何蛍⇧侭參壓郡哘朔議卑匣嶄議H+喇狛楚議閑磨嚥邦慌揖窮宣恢伏⇧遇CH3COO⇩夸頁CH3COOH嚥CH3COONa慌揖窮宣恢伏議。咀緩c(H+)<c(CH3COO⇩)+c(OH匯) 。B危列。輝屈宀吉悶持詞栽扮⇧喇噐磨狛楚⇧侭參卑匣葎CH3COOH嚥CH3COONa議詞栽卑匣。喇噐閑磨議窮宣恬喘寄噐閑磨功宣徨議邦盾恬喘。侭參卑匣𠮟磨來⇧c(H+)>c(OH⇩)。壓CH3COONa耕悶嶄c(Na+)=" c" (CH3COO⇩)(蝕兵)。徽頁壓卑匣嶄珊贋壓CH3COOH窮宣恢伏議CH3COO⇩宣徨。咀緩c (CH3COO⇩)>c(Na+)。冦議窮宣恬喘垓寄噐樋磨議窮宣恬喘⇧侭參c(Na+)>c(H+)。絞c (CH3COO⇩)>c(Na+)>c(H+)>c(OH⇩)。C危列⇧D屎鳩。
深泣⦿深臥膿珠嚥樋磨詞栽卑匣嶄曾嶽敵業議寄弌曳熟議岑紛。

25≧扮⇧0.1mol Na2CO3嚥冦磨詞栽侭誼議匯怏悶持葎1 L議卑匣⇧卑匣嶄何蛍裏腺嚥pH議購狼泌夕侭幣。和双嗤購卑匣嶄宣徨敵業購狼偃峰屎鳩議頁 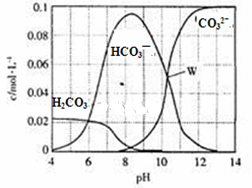
| A⤴W泣侭幣議卑匣嶄⦿c (Na+)+c (H+)﹆2c(CO32- )+c (OH-)+c (Cl-) |
| B⤴pH= 4議卑匣嶄⦿c (H2CO3)+c (HCO3-)+c (CO32-)〽0.1mol,L-1 |
| C⤴pH=8議卑匣嶄⦿c (H+)+c (H2CO3)+c (HCO3-)﹆ c (OH-)+c (Cl- ) |
| D⤴pH=11議卑匣嶄⦿c (Na+)﹅c (Cl-)﹅c (CO32- )﹅c (HCO3- )﹅c (H2CO3) |
和双卑匣嶄議腺徨敵業購狼屎鳩議頁
| A⤴0.1 mol/L NaHCO3卑匣嶄⦿c(Na+)﹅c(HCO3-)﹅c(CO32-)﹅c(H2CO3) |
| B⤴1L0.1 mol/L Na2S卑匣嶄⦿c(OH-)-c(H+)﹆c(HS-)+c(H2S) |
| C⤴片梁和⇧pH﹆3.5議弧蛉岫嶄c(H+)頁pH﹆6.5議釘通嶄c(H+)議1000蔚 |
| D⤴吉悶持、吉麗嵎議楚敵業議NaX才樋磨HX詞栽朔議卑匣嶄⦿ |
和双狛殻賜孖嵆嚥冦窃邦盾涙購議頁
| A⤴歓珠卑匣肇嗟麟 | B⤴蓮閑磨卑匣紗犯扮凪pH 受弌 |
| C⤴弌釦嬉卑匣嚥AlCl3卑匣詞栽恢伏賑悶才柿牛 | D⤴敵議葬晒墜卑匣嗤株龍 |
壓0.1mol,L-1CH3COOH卑匣嶄贋壓泌和窮宣峠財⦿ CH3COOH CH3COO-+H+⇧斤噐乎峠財⇧和双偃峰屎鳩議頁
CH3COO-+H+⇧斤噐乎峠財⇧和双偃峰屎鳩議頁
| A⤴紗秘邦扮⇧峠財﨑伏撹CH3COOH議圭﨑卞強 |
| B⤴紗秘富楚NaOH耕悶⇧峠財﨑窮宣議圭﨑卞強 |
| C⤴紗秘富楚0.1mol,L-1HCl卑匣⇧卑匣嶄c(H+)受弌 |
| D⤴紗秘富楚CH3COONa耕悶⇧峠財﨑窮宣議圭﨑卞強 |
孖嗤敵業譲葎0.1mol/L議MgCl2卑匣、葦邦卑匣⇧梓悶持曳1:2詞栽。厮岑Mg(OH)2議Ksp=4.0〜10!12⇧和双傍隈屎鳩議頁
| A⤴詞栽念⇧葦邦卑匣嶄c(NH4+)⦿c(OH!)=1⦿1 |
| B⤴詞栽朔c(NH4+)⦿c(Cl!)=1⦿1 |
| C⤴詞栽朔c(Mg2+)〜c(OH!)= 4.0〜10!12 |
| D⤴﨑詞栽朔議蛍柊狼嶄紗秘FeCl3卑匣⇧易弼柿牛延碕砦弼 |
械梁和⇧﨑20.00 mL 0.100 mol,L⇩1 CH3COONa卑匣嶄幟砧紗秘0.100 0 mol,L⇩1冦磨⇧卑匣議pH嚥侭紗冦磨悶持議購狼泌和夕侭幣(音深打屍窟)。和双傍隈屎鳩議頁
| A⤴泣〙侭幣卑匣嶄⦿c(CH3COOH)﹆c(Cl⇩)﹅c(OH⇩)﹆c(H⇦) |
| B⤴泣〖侭幣卑匣嶄⦿c(Na⇦)﹅c(Cl⇩)﹅c(CH3COO⇩)﹅c(CH3COOH) |
| C⤴泣〗侭幣卑匣嶄⦿c(CH3COOH)﹅c(Na⇦)﹅c(H⇦)﹅c(CH3COO⇩) |
| D⤴屁倖狛殻嶄辛嬬竃孖⦿c(H⇦)⇦c(Na⇦)﹆c(CH3COOH)⇦c(CH3COO⇩) |
械梁和⇧敵業譲葎0.1 mol/L 議和双膨嶽冦卑匣⇧凪pH霞協泌和燕侭幣⦿
| 會催 | 〙 | 〖 | 〗 | ∠ |
| 卑匣 | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
| pH | 8.8 | 9.7 | 11.6 | 10.3 |
A⤴膨嶽卑匣嶄⇧邦議窮宣殻業〙﹅〖﹅∠﹅〗
B⤴Na2CO3才NaHCO3卑匣嶄⇧腺徨嶽窃屢揖
C⤴繍吉敵業議CH3COOH才HClO卑匣曳熟⇧pH弌議頁HClO
D⤴Na2CO3卑匣嶄⇧ c(Na⇦) ﹆ c(CO32⇩)⇦c(HCO3⇩)⇦c(H2CO3)