��Ŀ����
����Ŀ���±���ǰ20��Ԫ���еIJ���Ԫ�ص�һЩ���ݣ�
A | B | C | D | E | F | G | H | I | J | |
ԭ�Ӱ뾶(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
���̬ | +6 | +1 | �� | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
��ͼ�̬ | -2 | �� | -2 | �� | -4 | -3 | -1 | �� | -3 | -4 |
�Իش��������⣺
(1)����10��Ԫ�ص縺��������_____(��Ԫ�ط���)����Ԫ��Bԭ��������7��Ԫ����Ԫ�����ڱ��е�λ�ã���_____���ڣ���_____�壬���̬ԭ�ӵĺ�������Ų�ʽ��________��
(2)H��I��J����Ԫ�ض�Ӧ���ʵ��۵��������ߵ�˳����(�õ��ʵľ��廯ѧʽ����)__________��
(3)Ԫ��E��C����Ԫ�ؿ��γ�һ����Է�������Ϊ60��һԪ������ӡ�������й��γ�________���Ҽ���________���м���
(4)I����Ԫ���γɵ�10���ӷ���X�Ŀռ乹��Ϊ________����X����ˮ�����Һ���뵽CuSO4��Һ�����������õ��������ӵĻ�ѧʽΪ________������X��Cu2+֮����_____________����ϡ�
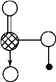
(5)��ͼ��IԪ���γɵĺ�����Ľṹ�����Ҫ˵��������������ˮ��ԭ��
a._________________________________��
b._________________________________��
(6) ��ͼ��J��E��ɵľ���ṹ����ÿ����J��Χ���Jԭ����ĿΪ_________���������߳�Ϊa cm��������ܶ�Ϊ_______________���ú�a��NA�Ĵ���ʽ��ʾ��(g/mL)��

���𰸡� O 4 VIII 1s22s22p63s23p63d64s2(��[Ar]3d64s2) N2 <Na< Si 7 1 ������ [Cu (NH3)4]2�� ��λ HNO3�Ǽ��Է��ӣ������ڼ��Ե�ˮ�� HNO3�����еģ�OH����ˮ����֮���γ���� 12 ![]() ��
�� ![]() ��
��![]()
��������ǰ20��Ԫ���У�AC������ͼ�-2������VIA�壬A��+6�ۣ�Cֻ��-2�ۣ���AΪS��CΪOԪ�أ�E��J����+4��-4�ۣ�����IVA�壬E��ԭ�Ӱ뾶��С����E��CԪ�ء�J��Si��F��I����+5��-3�ۣ�����VA�壬F��ԭ�Ӱ뾶����I����F��PԪ�ء�I��NԪ�أ�G��+7��-1�ۣ�Ϊ��A��Ԫ�أ�G��ClԪ�أ�Dֻ��+3�ۣ�Ϊ��A��Ԫ�أ�ԭ�Ӱ뾶����Siԭ�Ӱ뾶������D��AlԪ�أ�B��H�������Ϊ+1��û�и��ۣ�����IA�壬B��ԭ�Ӱ뾶��Alԭ�Ӱ뾶��ܶ࣬���ܴ���ͬ���ڣ���BΪK��B��Hԭ�Ӱ뾶����̫��Ӧ���ڣ���HΪNa��
(1)ͬ����������ҵ縺�Գ��������ƣ�ͬ�������϶��µ縺�Լ�С��������Ԫ���е縺������Ԫ������Ԫ�أ���Ԫ��Bԭ��������7��Ԫ��ΪFe�����ڵ�������VIII�壻��̬ԭ�Ӻ�������Ų�Ϊ��1s22s22p63s23p63d64s2(��[Ar]3d64s2)���ʴ���Ϊ��O��4��VIII��1s22s22p63s23p63d64s2(��[Ar]3d64s2)��
(2)HΪNa��I��N��J��Si���䵥�ʵ��۵��������ߵ�ΪN2��Na��Si���ʴ�Ϊ��N2��Na��Si��
(3)̼Ԫ�ء���Ԫ�ؼ���Ԫ�ؿ��γ�һ����Է�������Ϊ60��һԪ������ӣ�������ΪCH3COOH��������й��γ�7��������1���������ʴ�Ϊ��7��1��
(4)XΪNH3��NH3�е�ԭ�ӵļ۲���Ӷ���Ϊ![]() =4����һ�Թµ��Ӷԣ�����NH3�ռ乹��Ϊ�����Σ���NH3����ˮ�����Һ���뵽CuSO4��Һ�����������õ������ӵĻ�ѧʽΪ[Cu(NH3)4]2+������NH3��Cu2+֮������λ����ϣ��ʴ�Ϊ�������Σ�[Cu(NH3)4]2+����λ��
=4����һ�Թµ��Ӷԣ�����NH3�ռ乹��Ϊ�����Σ���NH3����ˮ�����Һ���뵽CuSO4��Һ�����������õ������ӵĻ�ѧʽΪ[Cu(NH3)4]2+������NH3��Cu2+֮������λ����ϣ��ʴ�Ϊ�������Σ�[Cu(NH3)4]2+����λ��
(5)ͼ1�еĺ�����ΪHNO3��HNO3������ˮ��ԭ��a��HNO3�Ǽ��Է��ӣ������ڼ��Ե�ˮ�У�b��HNO3�����е�-OH����ˮ����֮���γ�������ʴ�Ϊ��HNO3�Ǽ��Է��ӣ������ڼ��Ե�ˮ�У�HNO3�����е�-OH����ˮ����֮���γ������
(6)J��Si��E��C���Ծ��������ϵ�SiΪ������֮���������SiΪ12��������Siԭ����ĿΪ8��![]() +6��
+6��![]() =4��������Cԭ����ĿΪ4�������߳�Ϊacm���������Ϊa3��������ܶ�Ϊ
=4��������Cԭ����ĿΪ4�������߳�Ϊacm���������Ϊa3��������ܶ�Ϊ![]() g/mL=
g/mL=![]() g/mL=
g/mL=![]() g/mL���ʴ�Ϊ��12��
g/mL���ʴ�Ϊ��12�� ![]() ��
��![]() ��
��

 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�

