题目内容
4.酒后驾车是引发交通事故的重要原因.交警队对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液与乙醇迅速生成蓝绿色Cr3+.下列对乙醇的描述与此测定原理有关的是( )| A. | 乙醇有还原性 | B. | 乙醇发生了加成反应 | ||
| C. | 乙醇密度比水小 | D. | 乙醇是烃的含氧化合物 |
分析 根据乙醇沸点低,易挥发,故可以易被检测及乙醇具有还原性,K2Cr2C7具有强氧化性,可以氧化乙醇,自身生成Cr3+来分析解答.
解答 解:A.乙醇分子中含有羟基,具有还原性,K2Cr2C7具有强氧化性,可以把乙醇迅速氧化为乙酸蓝绿色的Cr3+,与测定原理有关,故A正确;
B.反应为氧化还原反应,不是加成反应,故B错误;
C.乙醇的密度大小与反应无关,故C错误;
D.乙醇可看成是乙烷中的氢原子被羟基取代后的产物,是烃的含氧化合物,与测定原理无关,故D错误.
故选A.
点评 本题主要考查乙醇的性质,难度不大,本题中的信息交警对驾驶员进行呼气酒精检测的原理是解答的关键,学生应学会信息的抽取和应用来解答习题.

练习册系列答案
相关题目
11.YBa2Cu8O2(Y为元素钇)是磁悬浮列车中的重要超导材料,下列关于${\;}_{39}^{59}Y$的说法不正确的是( )
| A. | 属于金属元素 | |
| B. | 质子数与中子数之差为50 | |
| C. | 原子的核外电子数是39 | |
| D. | ${\;}_{39}^{49}$Y和${\;}_{39}^{50}$Y是两种不同的核素 |
15.钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法正确的是( )

| A. | 该氧化物是含有非极性键的离子化合物 | |
| B. | 晶体的化学式为Ba2O2 | |
| C. | 该晶体晶胞结构与CsCl相似 | |
| D. | 晶体中Ba2+的配位数为8 |
12.丁香油酚的结构简式为: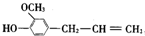 ,下列关于该有机物的说法中,正确的是( )
,下列关于该有机物的说法中,正确的是( )
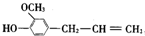 ,下列关于该有机物的说法中,正确的是( )
,下列关于该有机物的说法中,正确的是( )| A. | 丁香油酚的分子式为C10H10O2 | |
| B. | 丁香油酚易溶于水 | |
| C. | 丁香油酚能发生加成反应、加聚反应、取代反应 | |
| D. | 丁香油酚与苯酚互为同系物,可以和碳酸钠反应生成CO2 |
19.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,22.4L甲醇中含有的氧原子数为1.0NA | |
| B. | 常温常压下,46gNO2与 N2O4的混合气体中含有的原子总数为3NA | |
| C. | 标准状况下,2.24LCl2与足量的稀NaOH溶液反应,转移电子总数为0.2NA | |
| D. | 1L 1 mol•L-1的盐酸中,所含氯化氢分子数为NA |
9.mgH2O中含有1mol电子,则m的值为( )
| A. | 18g | B. | 1.8g | C. | 6g | D. | 0.6g |
16.氮化铝(AlN、Al和N的相对原子质量分别为27和14)广泛应用于电子、陶瓷等工业领域.在一定条件下,AlN可通过反应Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO合成.下列叙述正确的是( )
| A. | 上述反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | AlN的摩尔质量为41 g | |
| C. | AlN中氮元素的化合价为+3 | |
| D. | 上述反应中,每生成1 mol AlN需转移3 mol电子 |
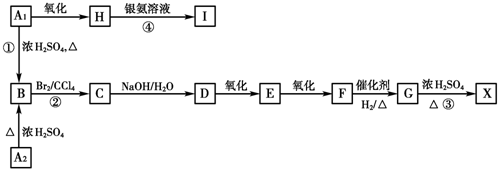
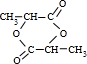 .
. .
.