题目内容
设nA为阿伏加德罗常数的数值,下列说法正确的是( )。
| A.常温常压下,8 g O2含有4nA个电子 |
| B.1 L 0.1 mol·L-1的氨水中有nA个NH4+ |
| C.标准状况下,22.4 L盐酸含有nA个HCl分子 |
| D.1 mol Na被完全氧化生成Na2O2,失去2nA个电子 |
A
解析

练习册系列答案
相关题目
设阿伏加德罗常数的值为,则下列说法正确的是 ( )
A.标准状况下,22.4 L乙烯含有的共用电子对数为2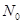 |
B.常温下,含有1 mol NaHSO4溶液中的阳离子数为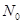 |
C.通常状况下,1 mol NO和0.5 molO2在密闭容器中混合,生成NO2分子数为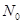 |
D.制取漂白粉时,标准状况下22.4 LCl2参加反应,转移电子数为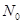 |
M(NO3)2热分解化学方程式为:2M(NO3)2 2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11.2L的气体,那么M的摩尔质量是
2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11.2L的气体,那么M的摩尔质量是
| A.24g/mol | B.74g/mol | C.148g/mol | D.40g/mol |
设NA为阿伏加德罗常数的数值,若等质量的H2O和D2O分别与一定质量的金属钾完全反应,转移的电子数均为 NA,则下列各量不相等的是( )
NA,则下列各量不相等的是( )
| A.消耗H2O和D2O的物质的量 |
| B.同温同压下生成气体的体积 |
| C.反应后所得溶液中溶质的质量分数 |
| D.参加反应的钾的质量 |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是 ( )。
| A.7.8 g Na2O2中含有的阴离子数为0.2NA |
| B.铜与浓硫酸反应中,当转移的电子数为0.2NA时,生成的SO2为2.24 L |
| C.1 mol·L-1的NH4Cl溶液中的NH4+的数目小于NA |
| D.由NO2、O2组成的混合物中共有NA个分子,其中的氧原子数目为2NA |
下列溶液中,溶质的物质的量浓度为1 mol/L的是( )
| A.将40 g NaOH溶于1 L水所得的溶液 |
| B.将80 g SO3溶于水并配成1 L的溶液 |
| C.将0.5 mol/L的NaNO3溶液100 mL加热蒸发掉50 g水的溶液 |
| D.含K+为2 mol的K2SO4溶液 |
某地酸雨经检验除含H+外[c(OH-)可以忽视]还有Na+、Cl-、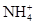 、
、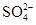 ,其浓度依次为:c(Na+)=2.3×10-5mol/L,c(Cl-)=3.5×10-5mol/L,
,其浓度依次为:c(Na+)=2.3×10-5mol/L,c(Cl-)=3.5×10-5mol/L,
c(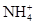 )=2.3×10-5mol/L,c(
)=2.3×10-5mol/L,c(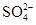 )=1.05×10-5mol/L。则该地酸雨的pH为( )
)=1.05×10-5mol/L。则该地酸雨的pH为( )
| A.3 | B.4 | C.5 | D.6 |
设NA代表阿伏加德罗常数的值,下列说法正确的是( )。
| A.1 mol甲基(—CH3)中含有的电子数为7NA |
| B.25 ℃时,pH=7的NH4Cl和NH3·H2O的混合溶液中,OH-数为10-7NA |
| C.42 g丙烯中含有的共价键数目为9NA |
| D.两份均为2.7 g的铝样品分别与100 mL浓度均为2 mol·L-1的盐酸和氢 |