��Ŀ����
�±�ΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��û�ѧ����ش��������⣺
(1)�ܢݢ�ԭ�Ӱ뾶��С�����˳��Ϊ(��Ԫ�ط��ű�ʾ) ��
�ڢۢߵ���ۺ����������������ǿ��˳����(�û�ѧʽ��ʾ) ��
(2)д��������ijЩԪ�ع��ɵļȺ����Ӽ����ֺ����Թ��ۼ��Ļ�����ĵ���ʽ(д��һ�ּ���) ��
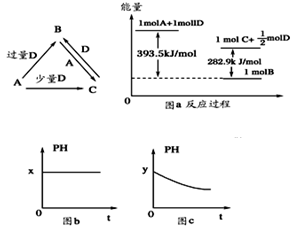
(3)��֪������1 g�ٵ����ڢܵ�����ȼ�������ȶ���Һ̬����ʱ�ų�142.9 kJ���������ʾ�ٵ���ȼ�յ��Ȼ�ѧ����ʽΪ ��
(4)�٢��γɵ���Ļ�������ܵ�����KOH���������Һʱ���γ�ԭ��أ����и����ĵ缫��ӦΪ ��
(5)�ɱ���Ԫ�آ٢ۢܢޢ����γɵij�������X��Y��Z��M��N�ɷ������·�Ӧ��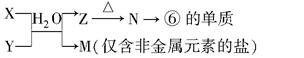
��X��Һ��Y��Һ��Ӧ�����ӷ���ʽΪ ��
��N���ĵ��������õķ����� ��
��M��Һ�����ԣ�ԭ����(�����ӷ���ʽ����) ��
(1)O��Al��Na��H2SiO3��H2CO3��HNO3
(2)  (�𰸺�������)(3)H2(g)��1/2O2(g)=H2O(l)��H����285.8 kJ��mol��1
(�𰸺�������)(3)H2(g)��1/2O2(g)=H2O(l)��H����285.8 kJ��mol��1
(4)CH4��8e����10OH��=CO32-��7H2O
(5)��Al3����3NH3��H2O=Al(OH)3����3NH4+
�ڵ�ⷨ ��NH4+��H2O NH3��H2O��H��
NH3��H2O��H��
����

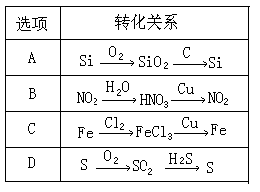
���г���I��II����ȷ�����������ϵ����
| ѡ�� | ����I | ����II |
| A | Fe3+�������� | ���ο�������ˮ�� |
| B | SiO2������������ | SiO2�ɺ�HF��Ӧ |
| C | Al2O3���۵�ܸ� | Al2O3�������ͻ���� |
| D | SO2��Ư���� | SO2��ʹ���������Һ��ɫ |
ij������M��ʽ��Ϊ80���׳ƺڷʱ�������ԭ������������20��X��Y��Z����Ԫ����ɣ�X��Y��Z��ԭ�����������������ϵΪZ=X+2Y��X��Y��ͬ�������ڵ�����Ԫ�ء�M����ˮ���ڳ�������ˮ���÷�������ˮ�⣬���ղ���Ϊһ�ְ�ɫ����A������B����������ʹʪ��ĺ�ɫʯ����ֽ������A�ڸ��������¿ɷֽ����һ��������ЧӦ�����塣��ע�����»ش����漰���������ʾ�����Ӧ�Ļ�ѧʽ��Ԫ�ط��ű�ʾ��
��1��������M�Ļ�ѧʽΪ ��Z��ԭ�ӽṹʾ��ͼΪ ��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��A�ڸ����·ֽ⣺ �� M��ˮ��Ӧ����A��B�� ��
��3��Z���⻯�����Ϊһ�ִ�����ϣ�д������ˮ��Ӧ�Ļ�ѧ����ʽ ��
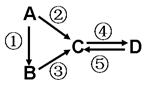
��4��������ϵ��о��ܹ㷺�����������У�����Ϊ������ϵ��� �������ţ�
| A��Ca(OH)2 | B��MgH2 | C��O2 | D��LaNi5 |
 ��ǿ�ᣩ����C��D�Ļ�����ͨ��NaOH��Һ��ǡ����ȫ��Ӧ�õ�һ���Σ������һ��ʵ�鷽���������е������� ��
��ǿ�ᣩ����C��D�Ļ�����ͨ��NaOH��Һ��ǡ����ȫ��Ӧ�õ�һ���Σ������һ��ʵ�鷽���������е������� ��