题目内容
氯气是一种重要的工业原料。工业上利用反应在3Cl2+8NH3=N2+6NH4Cl检查氯气管道是否漏气。下列说法正确的是
| A.若管道漏气遇氨就会产生白雾 | B.该反应利用了氨气的还原性 |
| C.该反应属于复分解反应 | D.生成6molNH4Cl有18mol电子转移 |
B
试题分析:氯气与氨气混合时发生氧化还原反应,生成白色的氯化铵固体小颗粒分散在空气中形成白烟,不可能产生白雾,因为液体小液滴分散在空气中才能形成白雾,故A项错误;氮元素由—3升为0价,发生氧化反应,则氨气是还原剂,显还原性,故B项错误;该反应前后氮、氯元素的化合价发生升降,而复分解反应中无元素化合价变化,故C项错误;根据元素化合价升降总数都是6,则3Cl2+8NH3=N2+6NH4Cl~6e-,该反应中氯化铵与转移电子的系数之比等于物质的量之比,生成6mol氯化铵时转移6mol电子,故D项错误。

练习册系列答案
相关题目
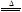 2KNO2+O2↑
2KNO2+O2↑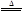 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑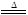 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑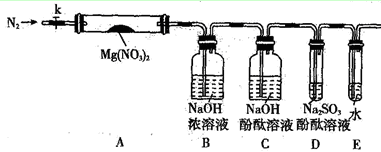


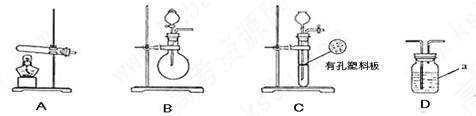
 .氧化铜反应后剩余固体的质量为
.氧化铜反应后剩余固体的质量为 .生成氮气在标准状况下的体积
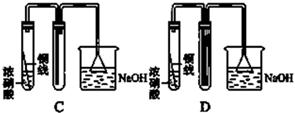
.生成氮气在标准状况下的体积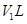 。乙小组测得洗气装置D前后的质量和生成氮气在标准状况下的体积。
。乙小组测得洗气装置D前后的质量和生成氮气在标准状况下的体积。 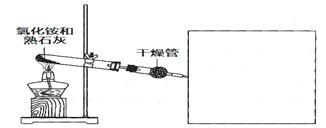
 2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
