题目内容
【题目】含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不正确的是( )
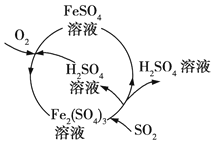
A. 该过程中可得到化工产品H2SO4
B. 该过程中化合价发生改变的元素为Fe和S
C. 该工艺流程是除去煤燃烧时产生的SO2
D. 图中涉及的反应之一为Fe2(SO4)3+SO2 + 2H2O=2FeSO4+2H2SO4
【答案】B
【解析】
由工艺流程可知,转化过程中吸收了氧气和二氧化硫,得到了化工产品硫酸。
A.由工艺流程图可以看出,转化过程中吸收了氧气和二氧化硫,排出了硫酸,所以该流程中可得到化工产品硫酸,故A正确;
B.该流程中化合价发生改变的元素有Fe、S和O,故B错误;
C.由工艺流程可知,二氧化硫被吸收生成了硫酸,所以该工艺流程是除去煤燃烧时产生的SO2,故C正确;
D.硫酸铁、水和二氧化硫反应生成硫酸亚铁和硫酸,所以图中吸收SO2的化学反应方程式为:Fe2(SO4)3+SO2 + 2H2O=2FeSO4+2H2SO4,故D正确,答案选B。

 名校课堂系列答案
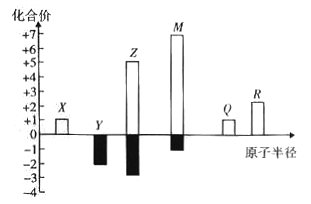
名校课堂系列答案【题目】A、B、C、D、E是五种短周期元素。已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等。甲、乙、丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子。
物质组成 | 甲 | 乙 | 丙 | 丁 |
化合物中各元素 原子个数比 | A和C 1:1 | B和A 1:4 | D和E 1:3 | B和E 1:4 |
请回答下列问题:
(1)若元素E的某种核素中中子数比质子数多3个,表示这种核素的符号为____________;
(2)把D的单质放到NaOH溶液中,反应的离子方程式为:_______________________;
(3)用电子式表示甲的形成过程:_____________________________________________;
(4)在密闭容器中充入BC2、BC和乙的混合气体共mg,若加入足量Na2O2,并不断用电火花点燃至反应完全,测得固体质量增重mg,则BC2与乙的质量比为________________;
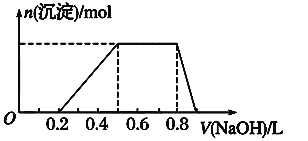
(5)有100mL MgCl2和丙的混合溶液,其中c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1 NaOH 溶液的体积是:____________mL。