题目内容
【题目】区别甲烷、乙烯、乙炔气体的最简易方法是
A. 分别通入溴水 B. 分别通入酸性高锰酸钾溶液
C. 分别在空气中燃烧 D. 分别通入盛有碱石灰的干燥管
【答案】C
【解析】A、乙烯、乙炔都能使溴水褪色,不能区分,A错误;B、乙烯、乙炔都能使酸性KMnO4溶液褪色,不能区分,B错误;C、甲烷、乙烯、乙炔三种气体中碳的含量依次升高,燃烧产生的现象依次为:淡蓝色火焰;明亮火焰,带有黑烟;明亮火焰,带有浓烟,可以区分,C正确;D、三种气体均与碱石灰不反应,不能区分,D错误,答案选C。

【题目】己知反应2FeCl3+Cu=CuCl2+2FeCl2 , 则下列判断正确的是( )
A.该反应是置换反应
B.该反应中FeCl3作还原剂
C.还原性:Cu>Fe2+
D.氧化性:CuCl2>FeCl3
【题目】25℃时,几种弱酸的电离平衡常数如下:
弱酸 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)CH3COOH、H2CO3、H2SO3三种酸中酸性最弱的是__________(填化学式)。
(2)CH3COOH的电离平衡常数表达式为K=__________。
(3)写出H2CO3的第二步电离方程式:_____________。
(4)写出H2SO3溶液和CH3COONa溶液反应的离子方程式:____________________。
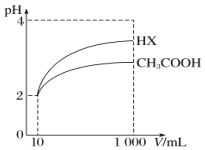
(5)将体积均为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH的变化如图所示,则HX的电离平衡常数____________(填“大于”“小于”或“等于”)醋酸的电离平衡常数,理由是__________________。