题目内容
9.现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2).要供选择的装置和药品如图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的).
(1)写出制取氮化镁的化学方程式3Mg+N2$\frac{\underline{\;\;△\;\;}}{\;}$Mg3N2 .
(2)连接并检查实验装置的气密性,实验开始时,打开自来水的开关,将空气从5升的储气瓶压入反应装置,则气流流经导管的顺序是(填入仪器接口字母编号)
(j)→( )( )→( )( )→( )( )→( )( )→(m)
(3)除装置A、E外,还应选择的装置(填字母代号)及其目的
| 装置 | 目的 |
(5)设计实验确定是否有氮化镁生成,写出实验操作、现象.将产物取少量置于试管中,加入适量水,将润湿的红色石蕊试纸置于试管口,如果能够看到润湿的红色石蕊试纸变蓝,则说明产物是氮化镁.
分析 (1)用氮气和镁在加热的条件下生成氮化镁,根据元素守恒可写出化学方程式;
(2)根据先除杂后干燥的原理及固体加热试管必须干燥的原理可将装置进行排序.气体参与的物质制备实验中装置的连接一般顺序是:制备气体→除杂→干燥→制备→尾气处理;
(3)根据题中信息可知Mg在空气中点燃可以和O2、CO2、H2O反应,所以镁和氮气反应必须将空气中的O2、CO2、H2O除去制得干燥纯净的N2,浓硫酸作用是除去水蒸气,浓氢氧化钠是除去空气中二氧化碳,还原粉为了除去空气中氧气,同时还应防止装置后面的空气中水进入装置与氮化镁反应;
(4)因为A装置没有排完空气前就加热会让空气中的氧气、CO2、水蒸气等与镁反应,如果装置F中的还原铁粉没有达到反应温度时,氧气不能除尽,导致氧同镁反应,而使氮化镁中混入氧化镁;
(5)取适量产物放入试管中,滴加蒸馏水,将润湿的红色石蕊试纸靠近试管口,如果试管中的溶液出现浑浊,红色石蕊试纸变蓝,则可以证明有氮化镁生成.
解答 解:(1)用氮气和镁在加热的条件下生成氮化镁,反应的方程式为3Mg+N2$\frac{\underline{\;\;△\;\;}}{\;}$Mg3N2 ,
故答案为:3Mg+N2$\frac{\underline{\;\;△\;\;}}{\;}$Mg3N2 ;
(2)气体参与的物质制备实验中装置的连接一般顺序是:制备气体→除杂→干燥→制备→尾气处理;所以除去空气中的O2、CO2、H2O制备氮化镁,装置连接顺序是,j→h→g→d→c→k→l(或l→k)→a→b (或b→a);
故答案为:j→h→g→d→c→k→l(或l→k)→a→b (或b→a);
(3)根据题中信息可知Mg在空气中点燃可以和O2、CO2、H2O反应,所以镁和氮气反应必须将空气中的O2、CO2、H2O除去制得干燥纯净的N2,浓硫酸作用是除去水蒸气,浓氢氧化钠是除去空气中二氧化碳,还原粉为了除去空气中氧气,同时还应防止装置后面的空气中水进入装置与氮化镁反应,所以除装置A、E外,还应选择的装置BDFG,各自的目的为
| 装置 | 目的 |
| B | 除去水蒸气 |
| D | 除去空气中的二氧化碳 |
| F | 除去空气中的氧气 |
| G | 吸收空气中的水蒸气 |
故答案为:
| 装置 | 目的 |
| B | 除去水蒸气 |
| D | 除去空气中的二氧化碳 |
| F | 除去空气中的氧气 |
| G | 吸收空气中的水蒸气 |
(4)因为A装置没有排完空气前就加热会让空气中的氧气、CO2、水蒸气等与镁反应,如果装置F中的还原铁粉没有达到反应温度时,氧气不能除尽,导致氧同镁反应,而使氮化镁中混入氧化镁,所以通气后,先点燃F处酒精灯,
故答案为:F;制得的氮化镁将不纯;
(5)依据氮化镁和水反应生成氨气,方程式为 Mg3N2+6H2O=3Mg(OH)2+2NH3↑,将产物取少量置于试管中,加入适量水,将润湿的红色石蕊试纸置于试管口,如果能够看到润湿的红色石蕊试纸变蓝,则说明产物是氮化镁;
故答案为:将产物取少量置于试管中,加入适量水,将润湿的红色石蕊试纸置于试管口,如果能够看到润湿的红色石蕊试纸变蓝,则说明产物是氮化镁.
点评 本题考查了物质实验室制备原理和装置选择,实验步骤的设计分析判断,物质性质的应用是解题关键,题目难度中等.

 特高级教师点拨系列答案
特高级教师点拨系列答案 某实验小组利用如下装置合成化工原料正丁醛.发生的反应如下:
某实验小组利用如下装置合成化工原料正丁醛.发生的反应如下:CH3CH2CH2CH2OH$→_{H_{2}SO_{4}加热}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO反应物和产物的相关数据列表如下:
| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.810 9 | 微溶 |
| 正丁醛 | 75.7 | 0.801 7 | 微溶 |
将6.0g Na2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸气出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在C中收集90℃以下的馏分.将馏出物倒入分液漏斗中,分去水层,再将有机层干燥、蒸馏后得正丁醛2.0g.回答下列问题:
(1)实验中不能将Na2Cr2O7溶液加到浓硫酸中的理由是浓硫酸溶于水会放出大量热,容易溅出伤人.
(2)加入沸石的作用是防止暴沸.
(3)分液漏斗使用前必须进行的操作是检查是否漏水.
(4)反应温度应保持在90~95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
(5)本实验中,正丁醛的产率为51.4%.
| A. | Na2CO3溶液 | B. | NaCl固体 | C. | NaOH溶液 | D. | CaCl2溶液 |
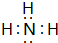 ;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).
;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).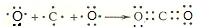 .
.