题目内容
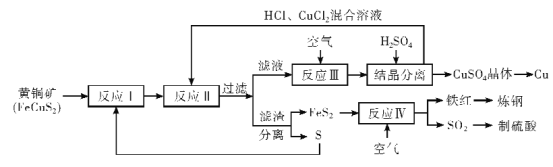
【题目】某工厂对制革工业污泥中Cr元素的回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+):
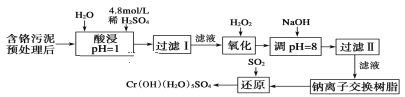
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | - | - | 4.7 | - |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
(1)酸浸时,为了提高浸取率可采取的措施是___(写一条即可)。
(2)调pH=8是为了除去___(填Fe3+、Al3+、Ca2+、Mg2+)。
(3)试配平氧化还原反应方程式:_Na2Cr2O7+_SO2+_H2O=________Cr(OH)(H2O)5SO4+_Na2SO4;每生成1molCr(OH)(H2O)5SO4消耗SO2的物质的量为___。
(4)印刷电路铜板腐蚀剂常用FeCl3。腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol/L,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中Fe3+ 和Fe2+的实验步骤:①___;②___;③过滤。(提供的药品:Cl2、浓H2SO4、NaOH溶液、CuO、Cu)。
【答案】升高温度、搅拌、过滤后再向滤渣中加入硫酸(多次浸取)、适当延长浸取时间 Fe3+、Al3+ 1 3 11 2 1 1.5mol 通入足量氯气将Fe2+氧化成Fe3+ 加入CuO调节溶液的pH至3.2~4.7
【解析】
硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+和Mg2+,双氧水有强氧化性,能氧化还原性的物质,Fe2+和Cr3+有还原性,Fe2+和Cr3+能被双氧水氧化为高价离子,以便于与杂质离子分离;加入NaOH溶液调pH=8,Fe3+、Al3+转化为沉淀除去;最后钠离子交换树脂交换的离子是钙离子和镁离子,据此分析。
硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+和Mg2+,双氧水有强氧化性,能氧化还原性的物质,Fe2+和Cr3+有还原性,Fe2+和Cr3+能被双氧水氧化为高价离子,以便于与杂质离子分离;加入NaOH溶液调pH=8,Fe3+、Al3+转化为沉淀除去;最后钠离子交换树脂交换的离子是钙离子和镁离子。
I、(1)酸浸时,为了提高浸取率可采取的措施是:升高温度、适当延长浸取时间、不断搅拌混合物、滤渣多次浸取等,
故答案为:升高温度、搅拌、过滤后再向滤渣中加入硫酸(多次浸取)、适当延长浸取时间;
(2)硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+和Mg2+,加入H2O2将Fe2+和Cr3+氧化,加入NaOH溶液调pH=8,Fe3+、Al3+转化为沉淀除去;
故答案为:Fe3+、Al3+;
(3)反应中,Na2Cr2O7中Cr元素的化合价由+6价降至Cr(OH)(H2O)5SO4中+3价,1molNa2Cr2O7得到6mol电子,S元素的化合价由+4价升至+6价,1molSO2失去2mol电子,根据得失电子守恒、原子守恒,配平后的方程式为:Na2Cr2O7+3SO2+11H2O=2Cr(OH)(H2O)5SO4+Na2SO4,
根据方程式:3SO2~2 Cr(OH)(H2O)5SO4
3 mol 2mol
n(SO2) 1mol
所以n(SO2)=1.5mol;
(4)根据上表给出的数据和提供的药品,除去CuCl2溶液中Fe3+和Fe2+的实验步骤是:通入足量的氯气将Fe2+氧化为Fe3+、加入CuO调节溶液pH值3.2~4.7使铁离子沉淀完全,然后过滤,
故答案为:①通入足量氯气将Fe2+氧化成Fe3+;②加入CuO调节溶液的pH至3.2~4.7。

【题目】(Ⅰ)如表是A、B两种有机物的有关信息:
A | B |
①分子模型为: ②能使溴的四氯化碳溶液褪色; ③其产量是衡量石油化工水平的标志。 | ①由C、H、O三种元素组成,是厨房中的常见调味剂; ②水溶液能使紫色石蕊试液变红。 |
根据表中信息回答下列问题:
(1)关于A的下列说法中,不正确的是_____(填标号)。
a.分子里含有碳碳双键 b.分子里所有的原子共平面 c.结构简式为CH2-CH2
(2)A与H2发生加成反应后生成X,与X在分子组成和结构上相似的有机物有一大类,它们的通式为CnH2n+2。当n=___时,这类机物开始出现同分异构休。
(Ⅱ)已知有机物A~F有如图转化关系:
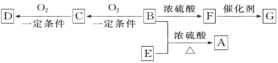
已知:①2CH3CHO+O2![]() 2CH3COOH+2H2O;
2CH3COOH+2H2O;
②CH3CH2OH![]() CH2=CH2↑+H2O(该反应属于消去反应)。
CH2=CH2↑+H2O(该反应属于消去反应)。
③A的分子式为C10H20O2; ④B分子中含2个甲基;⑤D、E互为具有相同官能团的同分异构体,D能与碳酸氢钠反应放出CO2,E分子烃基上的氢原子若被Cl取代,其一氯代物有3种;⑥F可以使溴的四氯化碳溶液褪色,G为高分子化合物。请填写以下空白:
(1)B可以发生的反应有_____(填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D分子所含有的官能团的名称是________。
(3)写出与D、E具有相同官能团的同分异构体(D、E除外)可能的结构简式______。
(4)写出下列转化的化学方程式:
B+E→A:_______;
B→C:___________;
F→G:__________。