题目内容
【题目】下列离子方程式正确的是( )
A.等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:Ba2++2OH+NH4++HCO3=BaCO3↓+NH3·H2O+H2O
B.将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
C.用铁电极电解氯化钠溶液:2Cl+2H2O![]() 2OH+H2↑+Cl2↑
2OH+H2↑+Cl2↑
D.将SO2通入Ca(ClO)2溶液中:Ca2++2ClO+SO2+H2O=CaSO3↓+2HClO
【答案】A
【解析】
A.等体积等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合,离子方程式:Ba2++2OH+NH4++HCO3=BaCO3↓+NH3·H2O+H2O,选项A正确;
B.磁性氧化铁中Fe元素的化合价![]() 为+2价,
为+2价,![]() 为+3价。磁性氧化铁溶于盐酸的离子方程式:Fe3O4+8H+=2Fe3++ Fe2++4H2O,选项B错误;
为+3价。磁性氧化铁溶于盐酸的离子方程式:Fe3O4+8H+=2Fe3++ Fe2++4H2O,选项B错误;
C.惰性电极电解氯化镁溶液的离子反应方程式为Mg2++2Cl-+2H2O![]() Cl2↑+H2↑+Mg(OH)2↓,选项C错误;
Cl2↑+H2↑+Mg(OH)2↓,选项C错误;
D.将SO2通入Ca(ClO)2溶液中的离子反应方程式为Ca2++ClO-+SO2+H2O═CaSO4↓+2H++Cl-,选项D错误;
答案选A。

【题目】含硼、氮、磷、铜、锌的化合物有许多重要用途。回答下列问题:
(1)基态B原子电子占据最高能级的电子云轮廓图为____;基态Cu+的核外电子排布式为___。
(2)化合物(CH3)3N能溶于水的原因是______。
(3)亚磷酸(H3PO3)是磷元素的一种含氧酸,与NaOH反应只生成NaH2PO3和Na2HPO3两种盐,则H3PO3分子的结构式为____。
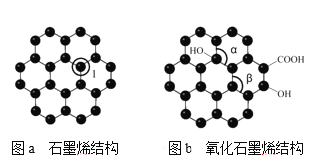
(4)Zn2+可与CN-、二苯硫腙(![]() )等形成稳定配合物。
)等形成稳定配合物。
①CN- 的结构式为_____。
②每个二苯硫腙分子中,采取sp2杂化的原子有__个。
(5)卤化锌的熔点如表所示:
ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
熔点/℃ | 872 | 275 | 394 | 446 |
ZnF2的熔点远高于其它三种卤化锌,其原因为_____。
(6)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图1所示:
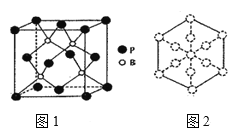
①磷化硼晶胞沿着体对角线方向的投影如图2,请在答题卡上将表示B原子的圆圈涂黑____。
②已知磷化硼晶体的密度为ρ g/cm3,阿伏加德罗常数为NA,则B—P键长为___pm(列出计算式即可)。
【题目】某工厂对制革工业污泥中Cr元素的回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+):
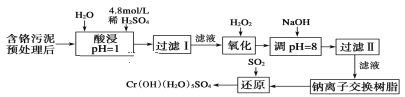
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | - | - | 4.7 | - |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
(1)酸浸时,为了提高浸取率可采取的措施是___(写一条即可)。
(2)调pH=8是为了除去___(填Fe3+、Al3+、Ca2+、Mg2+)。
(3)试配平氧化还原反应方程式:_Na2Cr2O7+_SO2+_H2O=________Cr(OH)(H2O)5SO4+_Na2SO4;每生成1molCr(OH)(H2O)5SO4消耗SO2的物质的量为___。
(4)印刷电路铜板腐蚀剂常用FeCl3。腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol/L,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中Fe3+ 和Fe2+的实验步骤:①___;②___;③过滤。(提供的药品:Cl2、浓H2SO4、NaOH溶液、CuO、Cu)。