题目内容
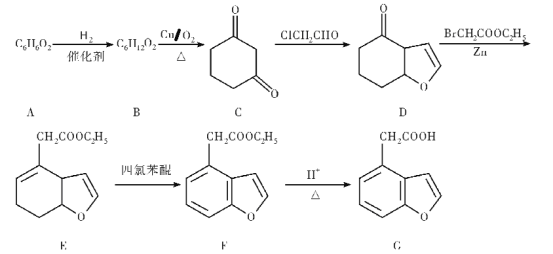
【题目】铜是人类最早使用![]() 金属,在生产生活中应用及其广泛。工业上以黄铜矿 (主要成分FeCuS2)为原料制取金属铜,其主要工艺流程如图所示。
金属,在生产生活中应用及其广泛。工业上以黄铜矿 (主要成分FeCuS2)为原料制取金属铜,其主要工艺流程如图所示。
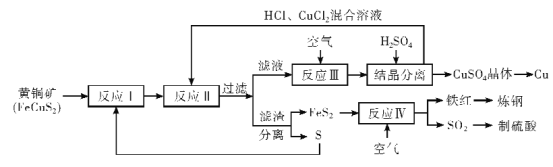
已知:反应II的离子方程式:Cu2++CuS+4Cl-=2[CuCl2]-+S
回答下列问题:
(1)FeCuS2中Fe的化合价__________。
(2)写出一条能使反应I充分进行的措施是_______________________________。
(3)反应III的离子方程式为_________________________________。向反应III后的溶液中加入稀硫酸结晶分离的具体操作为 ____________________。
(4)反应IV的化学方程式为____________________________________。反应IV中,也可以氨水吸收尾气SO2再制成化学肥料,写出氨水吸收SO2的化学方程式_________________
(5)该流程中,可循环利用的物质除CuCl2外,还有___________________(填化学式)。
【答案】+2 粉碎黄铁矿,或其他合理答案 4[CuCl2]-+O2+4H+=4Cu2++8Cl-+2H2O 蒸发浓缩冷却结晶过滤 4FeS2+11O2![]() 2Fe2O3+8SO2 2NH3 H2O +SO2=(NH4)2SO3 + H2O(或其他合理答案) HCl S H2SO4
2Fe2O3+8SO2 2NH3 H2O +SO2=(NH4)2SO3 + H2O(或其他合理答案) HCl S H2SO4
【解析】
在工艺流程中,反应Ⅰ为FeCuS2与S反应,生成FeS2和CuS;反应Ⅱ为CuS与CuCl2、HCl反应,Cu2++CuS+4Cl-=2[CuCl2]-+S;反应Ⅲ为[CuCl2]-与O2反应,生成CuCl2和HCl;反应Ⅳ为FeS2与O2反应,生成Fe2O3和SO2。
(1)FeCuS2中Cu显+2价,S显-2价,则Fe的化合价+2。答案为:+2;
(2)能使反应I充分进行的措施是粉碎铁矿石,或不断搅拌固体混合物;
(3)反应III的离子方程式为4[CuCl2]-+O2+4H+=4Cu2++8Cl-+2H2O;向反应III后的溶液中加入稀硫酸,将一部分CuCl2转化为CuSO4和HCl,结晶分离的具体操作为蒸发浓缩、冷却结晶、过滤。答案为:蒸发浓缩、冷却结晶、过滤;
(4)反应IV的化学方程式为4FeS2+11O2![]() 2Fe2O3+8SO2;反应IV中,也可以氨水吸收尾气SO2再制成化学肥料,氨水吸收SO2的化学方程式:2NH3 H2O+SO2=(NH4)2SO3+H2O。
2Fe2O3+8SO2;反应IV中,也可以氨水吸收尾气SO2再制成化学肥料,氨水吸收SO2的化学方程式:2NH3 H2O+SO2=(NH4)2SO3+H2O。
(5)该流程中,可循环利用的物质除CuCl2外,还有HCl、S、H2SO4。

【题目】某工厂对制革工业污泥中Cr元素的回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+):
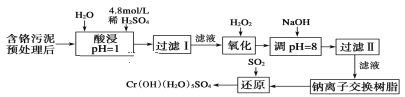
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | - | - | 4.7 | - |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
(1)酸浸时,为了提高浸取率可采取的措施是___(写一条即可)。
(2)调pH=8是为了除去___(填Fe3+、Al3+、Ca2+、Mg2+)。
(3)试配平氧化还原反应方程式:_Na2Cr2O7+_SO2+_H2O=________Cr(OH)(H2O)5SO4+_Na2SO4;每生成1molCr(OH)(H2O)5SO4消耗SO2的物质的量为___。
(4)印刷电路铜板腐蚀剂常用FeCl3。腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol/L,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中Fe3+ 和Fe2+的实验步骤:①___;②___;③过滤。(提供的药品:Cl2、浓H2SO4、NaOH溶液、CuO、Cu)。