题目内容
9. 钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:(1)钛有${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti两种原子,它们互称为同位素
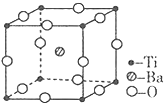
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如图所示,它的化学式是BaTiO3;
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如下:
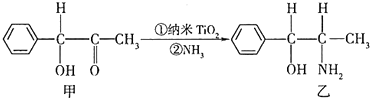
化合物乙中采取sp3杂化的原子的电负性由大到小的顺序为N>O>C
(4)有含Ti3+的配合物化学式为[TiCl(H2O)5]Cl2•H2O.配离子[TiCl(H2O)5]2+中含有的化学键类型是极性共价键和配位键,该配合物的配体是H2O、Cl-.
分析 (1)质子数相同、中子数不同的相同元素不同原子互为同位素;根据其价电子数及能层数确定在元素周期表中的位置,Ti元素核外有22个电子,根据构造原理书写其基态原子核外电子排布式;
(2)利用均摊法确定其化学式;
(3)采取sp3杂化的原子价层电子对数是4,同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素大于相邻元素;
(4)根据配合物的结构特点来分析其中的化学键以及配体情况.
解答 解:(1)2248Ti和2250Ti为质子数相同中子数不同的钛元素的不同原子,互称同位素,
故答案为:同位素;
(2)该化合物中,O原子个数=12×$\frac{1}{4}$,Ti原子个数=8×$\frac{1}{8}$,Ba原子个数为1,所以其化学式为:BaTiO3,
故答案为:BaTiO3;
(3)采取sp3杂化的原子价层电子对数是4,价层电子对个数是4的原子有:连接甲基和羟基的碳原子、氧原子和氮原子,同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素大于相邻元素,所以这三种元素第一电离能从大到小顺序是:N>O>C,
故答案为:N>O>C;
(4)配离子[TiCl(H2O)5]2+中含有非金属原子之间的极性共价键以及配位键,钛元素的配位体是H2O、Cl-,
故答案为:极性共价键、配位键;H2O、Cl-.
点评 本题考查物质结构和性质,涉及晶胞的计算、原子的杂化方式、第一电离能大小的判断、基态原子核外电子排布式的书写等知识点,这些都是高考热点,会利用价层电子对互斥理论确定原子的杂化方式、第一电离能的规律、构造原理来分析解答.

练习册系列答案
相关题目
19.在一定条件下向一密闭容器中充入2molSO2和1molO2,发生2SO2(g)+02(g)?2S03(g)的反应.下列有关说法正确的是( )
| A. | 单位时间内消耗2n molSO2的同时生成2n molS03,说明该反应达到平衡状态 | |
| B. | 达到化学平衡时,SO2、02和SO3的物质的量浓度均保持不变 | |
| C. | 达到化学平衡时,正反应和逆反应的速率都为零 | |
| D. | 达到化学平衡时,SO2将完全转化为SO3 |
20.实验室用溴和苯反应制取溴苯.得到粗溴苯后,要用如下操作精制:①蒸馏;②水洗;③用干燥剂干燥;④10%NaOH溶液洗.正确的操作顺序是( )
| A. | ①②③④② | B. | ②④①②③ | C. | ④②③①② | D. | ②④②③① |
17.某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取Cl2,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4 $\frac{\underline{\;\;△\;\;}}{\;}$2CaSO4+2Cl2↑+2H2O,他们设计了如下实验用于制取Cl2并验证其某些性质.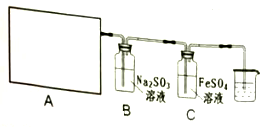
请回答:
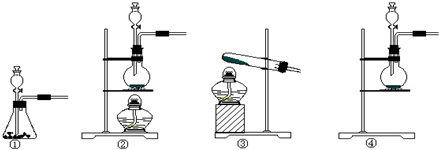
(1)该实验中A部分的装置是②(填写装置的序号).
(2)若要证明B中Na2SO3溶液已被氧化,所需要的化学试剂为BaCl2溶液、稀盐酸;
(3)实验进行了一段时间后,他们要探究C中FeSO4溶液被氧化的程度,设计了以下的方案,请填写其中的空白:
(4)完成酸性KMnO4溶液滴入FeSO4溶液中的离子反应方程式:
1Mn${O}_{4}^{-}$+5Fe2++8H+=1Mn2++5Fe3++4H2O.

请回答:
(1)该实验中A部分的装置是②(填写装置的序号).

(2)若要证明B中Na2SO3溶液已被氧化,所需要的化学试剂为BaCl2溶液、稀盐酸;
(3)实验进行了一段时间后,他们要探究C中FeSO4溶液被氧化的程度,设计了以下的方案,请填写其中的空白:
| 实验目的 | 操作与结论 |
| ①FeSO4溶液完全未被氧化 | 实验①取少许溶液于试管中,滴入数滴KSCN溶液,若溶液不变色(选填“不变色”或“变红色”),说明溶液完全未被氧化. |
| ②FeSO4部分被氧化 | ②实验②:取少许溶液于试管中,滴入数滴酸性KMnO4溶液,若溶液褪色;再另取少许溶液于试管中,滴加几滴KSCN溶液,溶液变 红(血红)色,说明溶液被部分氧化. |
| ③FeSO4完全被氧化 | ③重复实验②在待测②液中滴加数滴酸性KMnO4溶液后,溶液不褪色,另一实验现象与②同. |
1Mn${O}_{4}^{-}$+5Fe2++8H+=1Mn2++5Fe3++4H2O.
14.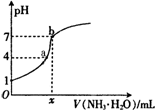 向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )
向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )
 向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )
向20.00mL稀H2SO4中逐滴加入0.10mol/L的氨水,测得溶液的pH随加入氨水的体积变化如图所示.下列判断正确的是( )| A. | x=20 | B. | 稀H2SO4的浓度为0.10mol/L | ||
| C. | b点有:2c(NH4+)=c(SO42-)>c(H+)=c(OH-) | D. | a点有:c(NH4+)<2c(SO42-) |
1.下列分子式表示的物质一定是纯净物的是( )
| A. | C5H10 | B. | CH4 | C. | C2H4O2 | D. | C2H4Cl2 |
18.下列物质的水溶液能够导电,但属于非电解质的是( )
| A. | 苯酚 | B. | 二氧化硫 | C. | 氯化氢 | D. | 氯气 |
19. (1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的热化学方程式为:
(1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的热化学方程式为:
a.C(s)+O2(g)═CO2(g)△H=E1①
b.C(s)+H2O(g)═CO(g)+H2(g)△H=E2②
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=E3③
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=E4④
请表达E1、E2、E3、E4之间的关系为E2=E1-E3-E4.
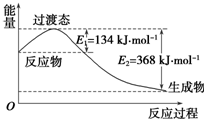
(2)如图所示是1摩尔NO2和1摩尔CO完全反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234 kJ•mol-1.
(3)化学反应的焓变与反应物和生成物的键能有关.已知某些化学键的键能如下表所示:
则反应:H2(g)+Cl2(g)═2HCl(g)的焓变△H=-185 kJ/mol.
 (1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的热化学方程式为:
(1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的热化学方程式为:a.C(s)+O2(g)═CO2(g)△H=E1①
b.C(s)+H2O(g)═CO(g)+H2(g)△H=E2②
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=E3③
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=E4④
请表达E1、E2、E3、E4之间的关系为E2=E1-E3-E4.
(2)如图所示是1摩尔NO2和1摩尔CO完全反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234 kJ•mol-1.
(3)化学反应的焓变与反应物和生成物的键能有关.已知某些化学键的键能如下表所示:
| 共价键 | H-H | Cl-Cl | H-Cl |
| 键能/(kJ•mol-1) | 436 | 247 | 434 |