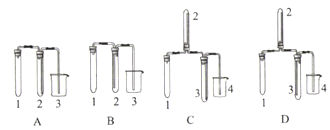
��Ŀ����
����Ŀ������Ȼ��Ϊԭ�Ϻϳɼ״����й��Ȼ�ѧ����ʽ���£�
��2CH4(g)+O2(g)==2CO(g)+4H2(g) ��H1=-70.8kJmol-1
��CO(g)+2H2(g)![]() CH3OH(g) ��H2
CH3OH(g) ��H2
��2CH4(g)+O2(g)![]() 2CH3OH(g) ��H3=-251.0 kJmol-1
2CH3OH(g) ��H3=-251.0 kJmol-1
��1����Ӧ������H2=________kJmol-1��
��2��������ɱ���ܱ�������Ͷ��1 mol CO��2 mol H2���ڲ�ͬ�����·�����Ӧ��CO(g)+2H2(g)![]() CH3OH(g)��ʵ����ƽ��ʱCH3OH�����ʵ������¶ȡ�ѹǿ�仯��ͼ1��ʾ��
CH3OH(g)��ʵ����ƽ��ʱCH3OH�����ʵ������¶ȡ�ѹǿ�仯��ͼ1��ʾ��

��M ��ʱ��H2 ��ת����Ϊ_________��ѹǿ�� p1_______���>����<����=����p2��
����Ӧ������N ��v��(CO) _______���>����<����=����M ��v ��(CO)
����ѹǿΪp1����1L�����ܱ������н���������Ӧ����ʼͶ�ϲ��䣩���ڲ�ͬ�¶���������Ӧ��ƽ�ⳣ���Ķ���(IgK)��ͼ2��ʾ�����¶�Ϊ506Kʱ��ƽ�ⳣ��K=____________�� B��C��D��E�ĵ�������ȷ��ʾ�÷�Ӧ��1gK ��T�Ĺ�ϵ�ĵ�Ϊ________________��
������2L�����ܱ������г���x (x>0)mol H2��2 mol CO����8 mol CH3OH(g)���� 506 K�½���������Ӧ��Ϊ��ʹ�÷�Ӧ������У�x�ķ�ΧΪ________________��
��3��ij�״�-����ȼ�ϵ����KOH��ҺΪ�������Һ����KOHȫ��ת����KHCO3ʱֹͣ�ŵ���д����ʱ�����ĵ缫��Ӧʽ______________________________��
���𰸡� -90.1 50% > < 1 BE 0<x<4 CH3OH+7OH--6e-=HCO3-+5H2O
��������������Ҫ����Ӱ�컯ѧƽ������������ƽ�ⳣ���ļ���ȡ�
��1����/2-��/2�÷�Ӧ�ڵ���H2=(��H3-��H1)/2=-90.1kJmol-1��
��2����M��ʱ������0.5mol CH3OH����1mol H2��H2��ת����Ϊ1/2=50%����ѹƽ�����ƣ�CH3OH�����ʵ�������p1ʱCH3OH�����ʵ����ϴ�����ѹǿ��p1>p2��
��M��N���¶���ͬ��M��ѹǿ�ϴ����Է�Ӧ���ʣ�N��v��(CO) <M��v��(CO)��
���¶�Ϊ506Kʱ��1gK=0��ƽ�ⳣ��K=0���÷�ӦΪ���ȷ�Ӧ��K�����¶����߶���С������B��C��D��E�ĵ�������ȷ��ʾ�÷�Ӧ��1gK��T�Ĺ�ϵ�ĵ�ΪBE��
����ʼŨ��c(CO)=1mol/L��c(H2)=0.5xmol/L��c(CH3OH)=4mol/L��Ũ����Q=![]() =16/x2��Ϊ��ʹ�÷�Ӧ������У�Ҫ��Q>K����16/x2>1��x�ķ�ΧΪ0<x<4��
=16/x2��Ϊ��ʹ�÷�Ӧ������У�Ҫ��Q>K����16/x2>1��x�ķ�ΧΪ0<x<4��
��3��KOHȫ��ת����KHCO3����ʱ�����ĵ缫��ӦʽCH3OH+7OH--6e-=HCO3-+5H2O��

 ��У����ϵ�д�
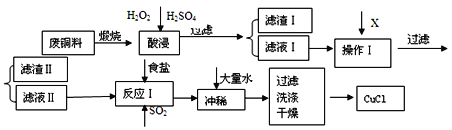
��У����ϵ�д�����Ŀ��CuCl���л��ϳɵ���Ҫ���������������ϡ������ȹ�ҵ����ҵ���ɷ�ͭ�ϣ���Fe��Al���仯���SiO2���ʣ�������CuCl�Ĺ����������£�
���� | ��ʼ���� | ������ȫ |
Fe(OH)3 | 2.7 | 3.7 |
Cu(OH)2 | 5.6 | 6.7 |
Al(OH)3 | 3.8 | 4.7 |
��֪��CuCl����NaCl��Ũ��Һ������CuCl2-��CuCl2-����Һ��ˮϡ�ͺ������CuCl������
��1�����յ���ҪĿ������______________________________________��
��2��������Ϊ������Һ��pHֵ����ΧΪ___________�����������X������_________________________ ��
A.CuO B.Cu(OH)2 C .NaOH ��Һ D.CaCO3
��3������I����Ҫ�ɷ���________�����������Ҫ�ɷ���_________��
��4������Һ���м���ʳ�β�ͨ��SO2������CuCl����д����Ӧ�����ӷ���ʽ________________________________________________________________________________________ ��
��5���ڷ�Ӧ���У����Ȳ�ʹ��ŨNaC1��Һ����ҪĿ����_____________________________________________________________________________________ ��
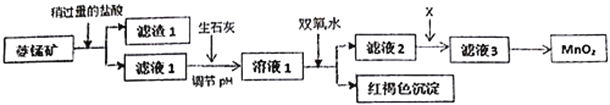
����Ŀ����ҵ�������̿�MnCO3���ۺ�FeCO3��SiO2��Cu2(OH)2CO3�����ʣ�Ϊԭ����ȡ�������̣�������ʾ��ͼ���£�
��֪�������������������pH
Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
��ʼ����ʱ | 8.3 | 6.3 | 2.7 | 4.7 |
��ȫ����ʱ | 9.8 | 8.3 | 3.7 | 6.7 |
Ksp(CuS)=6.3��10-16 Ksp(MnS)= 3��10-14
ע���������ӵ���ʼŨ��Ϊ0.1 mol/L
�ش��������⣺
��1�������ʵ����̿�ʹ��ǰ�轫����飬��ҪĿ����_________________________������1�ijɷ���_________�������ܽ�MnCO3�����ӷ���ʽ��_________________________________��
��2������ʯ�Ҷ�����NaOH����pH��ԭ����_______________________________��
��3����Һ2�м���ij������X���Գ�ȥCu2+�����ʺϵ���_______________��
A.MnO2 B.NaOH C.MnS
�÷�Ӧ�����ӷ���ʽ��____________________________��
��4����MnCl2ת��ΪMnO2��һ�ַ����ǽ��ữ��NaClO3��Һ����Mn2+���벹�䲢��ƽ���з��̣�____Mn2++_____ClO3-+______��____Cl2��+____MnO2+_________��_________________
��5����MnCl2ת��ΪMnO2����һ�ַ����ǵ�ⷨ�����������������������������������
�� MnO2�ڵ��ص�__________________������������������������������������ɣ�
�� ��ֱ�ӵ��MnCl2��Һ������MnO2��ͬʱ���������Cl2������Cl2�IJ�����_______________��