题目内容
(8分) 已知某反应A(g)+B(g)?C(g)+D(g)进行过程中的能量变化如图所示,请回答下列问题:
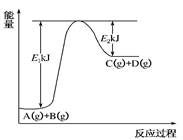
(1)该反应的ΔH=________kJ·mol-1(用含E1、E2的代数式表示)。(1分)
(2)若在反应体系中加入催化剂使逆反应速率增大,则E1________(填“增大”、“减小”或“不变”,下同),ΔH________。(2分)
(3)在相同温度和压强下,对反应A(g)+B(g)??C(g)+D(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表:
上述四种情况达到平衡后,C(D)的大小顺序是________。(2分)
A.乙=丁>丙=甲 B.乙>丁>甲>丙 C.丁>乙>丙=甲 D.丁>丙>乙>甲
(4)若上述反应达到平衡,为了提高A的转化率,可以采用的措施有(写一条):________________________________________________________________________。(1分)
(5)在恒温恒容条件下进行上述反应。下列情况可以判断该反应达到平衡状态的是____(2分)
A.气体平均摩尔质量不再变化 B. 气体压强不再变化
C. 气体密度不再变化 D. 消耗A的速率等于消耗D的速率
E. 各组分浓度之比为1:1:1:1 F. C生成的速率等于B消耗的速率

(1)该反应的ΔH=________kJ·mol-1(用含E1、E2的代数式表示)。(1分)
(2)若在反应体系中加入催化剂使逆反应速率增大,则E1________(填“增大”、“减小”或“不变”,下同),ΔH________。(2分)
(3)在相同温度和压强下,对反应A(g)+B(g)??C(g)+D(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表:
| | A | B | C | D |
| 甲 | a mol | a mol | 0 | 0 |
| 乙 | 2a mol | a mol | 0 | 0 |
| 丙 | a mol | a mol | a mol | a mol |
| 丁 | a mol | 0 | a mol | a mol |
A.乙=丁>丙=甲 B.乙>丁>甲>丙 C.丁>乙>丙=甲 D.丁>丙>乙>甲
(4)若上述反应达到平衡,为了提高A的转化率,可以采用的措施有(写一条):________________________________________________________________________。(1分)
(5)在恒温恒容条件下进行上述反应。下列情况可以判断该反应达到平衡状态的是____(2分)
A.气体平均摩尔质量不再变化 B. 气体压强不再变化
C. 气体密度不再变化 D. 消耗A的速率等于消耗D的速率
E. 各组分浓度之比为1:1:1:1 F. C生成的速率等于B消耗的速率
(1)E1-E2 (2)减小 不变 (3)A (4)升高温度、增加B的浓度 (5)D
该题为反应热与化学反应速率、化学平衡相结合的题目。(1)ΔH=E(反应物)-E(生成物)=E1-E2;(2)使用催化剂,减小反应的活化能,同时减小E1和E2,反应热不变;(3)首先用极端转化,将生成物全部转化为反应物,甲和丙,乙和丁是相同的。乙中2amol可以变为amol+amol;先通入amolA和amolB与甲完全相同,再通入amol,在甲的基础上平衡正向移动,故D的浓度,乙>甲,选A;(4)要提高A的转化率,可以使平衡正向移动。升高温度或增加B的浓度都可以。(5)判断平衡状态两点:υ正=υ逆、各物质的量保持不变,总结成改变的量如果不变了,即达到平衡。M=、ρ=、P在整个反应过程中均不变,F中只有正方向,故答案选D。

练习册系列答案
相关题目
 CH3OH(g) ΔH=-90.8 kJ·mol-1K1
CH3OH(g) ΔH=-90.8 kJ·mol-1K1 C(s)=
C(s)= 3.5kJ·mol-1 则2Fe(s)+
3.5kJ·mol-1 则2Fe(s)+