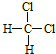��Ŀ����
����Ŀ�����������л������ϩ ��2-���� �ۼױ� ����Ȳ�����У�
��1���ܺ���һ�����ҵ�ʯ�ͻ�������ˮƽ����____________(����ţ���ͬ���������ʿ�����һ�ֳ������ϣ��䷴Ӧ�Ļ�ѧ����ʽ��_____________________________________________________��
��2����������ȡ�ݶ��ݣ�TNT������______________��
��3��̼Ԫ�ص������ٷֺ�����ߵ���________��ʵ������ȡ�����ʵķ�Ӧװ�����£�

�ټ��з�Ӧ�Ļ�ѧ����ʽ��_____________________________________________________ ��
�ڵμӱ���ʳ��ˮ����ֱ�ӵμ�ˮ��ԭ����________________________________________��
����������ͭ��Һ��������______________________________________________________��
���𰸡��� nCH2=CH2![]()
![]() �� �� CaC2 +2H2O��Ca(OH)2 +HC��CH�� ������Ӧ���� ��ȥ��Ȳ�е��������������
�� �� CaC2 +2H2O��Ca(OH)2 +HC��CH�� ������Ӧ���� ��ȥ��Ȳ�е��������������
��������
��1������һ������ʯ�ͻ�������ˮƽ�ı�־Ϊ��ϩ���ʢ���ȷ����ϩ�к���̼̼˫������ͨ���Ӿ۷�Ӧ�õ��߷��ӻ��������Ӧ����ʽΪnCH2=CH2![]()
![]() ��
��
��2��TNTΪ�������ױ�����ȡ�������ױ����ױ���Ũ������Ũ���Ტ���ȵ������½��У��ʢ���ȷ��
��3������ʵ��װ�ã����������õ�ʯ��ʳ��ˮ�Ʊ���CaC2��2H2O��Ca(OH)2��C2H2������������������к�̼����ߵ�����Ȳ��
�ٵ�ʯ��H2O��Ӧ�Ʊ���Ȳ���䷴Ӧ����ʽΪCaC2��2H2O��Ca(OH)2��C2H2����
�ڵ�ʯ��ˮ��Ӧ���ң����ʵ���ҳ��ñ���ʳ��ˮ����ˮ��Ŀ���Ǽ�����Ӧ���ʣ�
����Ȳ�л���H2S���壬CuSO4��H2S=CuS����H2SO4���������ͭ��Ŀ���dz�ȥ��Ȳ�����H2S��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��300��ʱ��������X������Y��0.16 mol����10 L�����ܱ������У�������Ӧ��X(g) +Y(g)![]() 2Z(g) ��H��0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g) ��H��0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
�ش��������⣺
��1����Ӧ0~2 min Z��ƽ������v(Z)=_____________
��2�����жϸ÷�Ӧ�Ѿ��ﵽƽ��״̬����_____________
A������X������������Z�����ʵ�2��
B��������ѹǿ���ֲ���
C��������������ܶȱ��ֲ���
D�������ڸ������Ũ�ȱ��ֲ���
��3��Ҫ���������Ӧ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��_____________����дһ�֣���
��4���¶�Ϊ300��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K��_______________
��5������ʼʱ��������г���X��Y��Z��0.20 mol����Ӧ����____����������������������Ӧ������У���ƽ��ʱZ���������������ƽ�����______������������������С��������������
����Ŀ��NaClO��Ư��Һ����Ч�ɷ֣�ij�о�С��̽��NaClO��Һ�����ʣ����������ʵ�飺
װ��ͼ | �Լ�X | ʵ������ | |
| �� | 0.2molL-1���� | ��������ɫ���� |
�� | 0.2molL-1KI-������Һ | ��Һ���� | |
�� | 0.2molL-1FeSO4(H+)��KSCN�����Һ | ��Һ��� | |
�� | 0.2molL-1AlCl3��Һ | ������ɫ���� | |
�����жϲ���ȷ����
A.ʵ����з����ķ�Ӧ��ClO-+Cl-+2H+��Cl2��+H2O
B.ʵ����з����ķ�Ӧ��ClO-+2I-+2H+��Cl-+I2+H2O
C.ʵ����и�������������ǿ����ClO-��Fe3+
D.ʵ�����ClO-��Al3+��ٽ�ˮ��
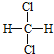
����Ŀ��ʵ�����Ʊ�1,2-���������ʵ���������£�
![]()
��֪������Ҫ����Ӧ���Ҵ���Ũ����Ĵ�������l40����ˮ�������ѡ�
���й������б����£�
�Ҵ� | 1,2-�������� | ���� | |
״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
�ܽ��� | ������ˮ | ������ˮ | ������ˮ |
�е㣯�� | 78.5 | 132 | 34.6 |
�Իش��������⣺
��1���Ҵ���Ũ����l70�淢����Ӧ�Ļ�ѧ����ʽ��______________________��
��2���Ҵ���Ũ���ᷴӦװ���з��뼸Ƭ���Ƭ��Ŀ����_________________________��
��3����Ӧ�õ��Ļ�������к���SO2��CO2�����壬�������е�SO2�����ѡ�õ��Լ���_______________________________��
��4�����ղ����У�Ӧ�ʵ���������Һ���¶ȣ�����ҪĿ����______________��
��5��ʵ���Ƶõ�1,2-��������ֲ�Ʒ�к�������δ��Ӧ��Br2����������Ʒ���ѣ�ijͬѧ��һ���ᴿ���£�
��� | ʵ�鷽�� | ʵ��Ŀ�Ļ���� |
�� | ��ȥ�ֲ�Ʒ������δ��Ӧ��Br2��ʵ�鷽����_________________ | ��ȥ������ |
�� | ��ȥ�ֲ�Ʒ�е����ѵ�ʵ�鷽���ǽ���ʵ�����л���������________________________ | ��ȥ�������� |