题目内容
19.下列说法正确的是( )| A. | 乙烯使溴水或酸性高锰酸钾褪色均属于加成反应 | |
| B. | 用乙醇与浓硫酸加热至170℃制乙烯的反应属于取代反应 | |
| C. | 用“地沟油”生产生物柴油只发生酯化反应 | |
| D. | 用重铬酸钾溶液检验司机是否酒驾所发生的反应属于乙醇的氧化反应 |
分析 A.乙烯中的碳碳双键能够被酸性高锰酸钾溶液氧化,该反应不属于加成反应;
B.乙醇制取乙烯的反应为消去反应;
C.用“地沟油”生产生物柴油过程中主要发生酯的水解反应;
D.乙醇被重铬酸钾溶液氧化生成乙酸.
解答 解:A.乙烯含有碳碳双键,与溴水发生加成反应,而使酸性高锰酸钾溶液褪色是氧化反应,故A错误;
B.用乙醇与浓硫酸加热至170℃制乙烯的反应属于消去反应,不是取代反应,故B错误;
C.用“地沟油”生产生物柴油主要发生酯的水解反应,不属于酯化反应,并且还有其它反应发生,故C错误;
D.乙醇被重铬酸钾溶液氧化生成乙酸,所以该反应属于氧化反应,故D正确;
故选D.
点评 本题考查乙烯、乙醇的性质,题目难度中等,明确物质中官能团与性质的关系是解本题关键,注意掌握取代反应、加成反应、消去反应的区别.

练习册系列答案
相关题目
9.现有部分短周期元素的性质或原子结构如下表:
(1)写出元素X的离子结构示意图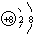 .写出元素Z的气态氢化物的电子式
.写出元素Z的气态氢化物的电子式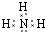 (用元素符号表示)
(用元素符号表示)
(2)写出Y元素最高价氧化物对应水化物的电离方程式H++AlO2-+H2O?Al(OH)3?Al3++3OH-
(3)元素T与氯元素相比,非金属性较强的是F(用元素符号表示),下列表述中能证明这一事实的是C.
A.常温下氯气的颜色比T单质的颜色深
B.T的单质通入氯化钠水溶液不能置换出氯气
C.氯与T形成的化合物中氯元素呈正价态
(4)探寻物质的性质差异性是学习的重要方法之-.T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是Al,理由具有金属性.
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | K电子数比L层电子数少4个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
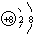 .写出元素Z的气态氢化物的电子式
.写出元素Z的气态氢化物的电子式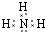 (用元素符号表示)
(用元素符号表示)(2)写出Y元素最高价氧化物对应水化物的电离方程式H++AlO2-+H2O?Al(OH)3?Al3++3OH-
(3)元素T与氯元素相比,非金属性较强的是F(用元素符号表示),下列表述中能证明这一事实的是C.
A.常温下氯气的颜色比T单质的颜色深
B.T的单质通入氯化钠水溶液不能置换出氯气
C.氯与T形成的化合物中氯元素呈正价态
(4)探寻物质的性质差异性是学习的重要方法之-.T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是Al,理由具有金属性.
10.“绿色化学”是指从技术、经济上设计可行的化学反应或化工设备,尽可能地节约能源,或尽可能减少对环境的负作用.下列选项中不符合绿色化学概念的是( )
| A. | 工业生产硫酸、硝酸的设备中安装热交换器 | |
| B. | 消除制硝酸工业尾气的氮氧化物污染:NO+NO2+2NaOH═2NaNO2+H2O | |
| C. | 消除硫酸厂尾气中的SO2:SO2+2NH3•H2O═(NH4)2SO3+H2O | |
| D. | 用废铜屑制CuSO4:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O |
7.下列物质中,都不能与Ag(NH3)2OH溶液发生银镜反应的一组是( )
①福尔马林;②蚁酸;③甲酸乙酯;④乙酸甲酯;⑤甲酸钠;⑥醋酸;⑦葡萄糖;⑧蔗糖;⑨麦芽糖.
①福尔马林;②蚁酸;③甲酸乙酯;④乙酸甲酯;⑤甲酸钠;⑥醋酸;⑦葡萄糖;⑧蔗糖;⑨麦芽糖.
| A. | ①②③④ | B. | ④⑥⑧ | C. | ⑦⑧⑨ | D. | ⑤⑥⑦⑧ |
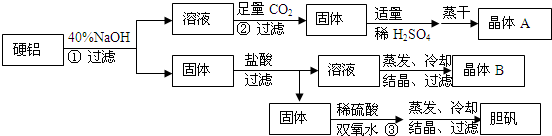
4.X、Y、Z均为中学化学常见物质,在一定条件下,X能与强酸或强碱溶液发生如下图的反应(部分反应物、生成物及反应条件略去).则下列说法不正确的是( )
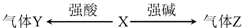
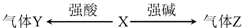
| A. | 若X为金属单质,则Y、Z可能为同一物质 | |
| B. | 若X为盐,则Y在标况下的密度一定是1.96g•L-1 | |
| C. | 若X为盐,则Z一定能使湿润的红色石蕊试纸变蓝 | |
| D. | 若X为盐,则其水溶液中水的电离程度比同温度下纯水的电离程度大 |
11.下列装置所示的实验中,能达到实验目的是( )
| A. | 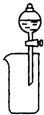 CCl4萃取I2后从下口放出水层 | B. | 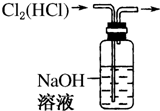 除去Cl2中的HCl | ||
| C. | 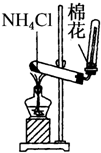 实验室制氨气 | D. | 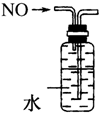 排水法收集NO |
8.下列有关电池及能源的叙述正确的是( )
| A. | 锌锰干电池工作一段时间后碳棒变细 | |
| B. | 铅蓄电池工作一段时间后酸性会增强 | |
| C. | 水和水煤气都是一级能源 | |
| D. | 铁与H2SO4反应时,加入少量CuSO4溶液时,可使反应加速 |
9.下列说法正确的是( )
| A. | 56g N2与12g H2在密闭容器中反应,转移电子的数目为12.0×6.02×1023. | |
| B. | 标准状况下,22.4L NO和11.2L O2混合后气体的分子总数为6.02×1023 | |
| C. | 工业上用电解法进行粗铜精炼时,每转移1mol电子,阳极上溶解的铜原子必为0.5×6.02×1023 | |
| D. | V L a mol•L-1 氯化铁溶液中,若Fe3+的数目为6.02×1023,则Cl-的数目大于3×6.02×1023 |