题目内容
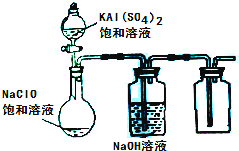 (2013?达州模拟)NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业.
(2013?达州模拟)NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业.(1)工业上可用氯化钠为原料,通过电解的方法制得NaClO,工业上制取NaClO的离子反应方程式为
Cl-+H2O
ClO-+H2↑
| ||
Cl-+H2O
ClO-+H2↑
电解后的溶液PH
| ||
大于
大于
7(填大于、小于、等于);其原因是ClO-+H2O?HClO+OH-
ClO-+H2O?HClO+OH-
(用离子方程式表示)(2)KAl(SO4)2溶液中质子守恒等式为
c(H+)=c(OH-)+3c(Al(OH)3)
c(H+)=c(OH-)+3c(Al(OH)3)
(3)某小组同学用下图所示装置探究饱和NaClO和KAl(SO4)2溶液混合反应的实验.
①打开活塞向烧瓶中加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀.此时反应的离子方程式为
3Cl-+Al3++3H2O=3HClO+Al(OH)3↓
3Cl-+Al3++3H2O=3HClO+Al(OH)3↓
.②将烧瓶中的混合液在阳光照射下,不久烧瓶中有黄绿色气体产生,充分反应后集气瓶中收集到一种无色无味的气体.写出在光照射下混合液中反应的化学方程式是4HClO
2H2O+2Cl2↑+O2↑
| ||
4HClO
2H2O+2Cl2↑+O2↑
.
| ||
(4)若将分液漏斗中的KAl(SO4)2溶液换成硫酸亚铁铵(一种复盐:(NH4)2SO4?FeSO4)溶液,其他不变.打开分液漏斗活塞向烧瓶中滴入足量的硫酸亚铁铵溶液.观察到烧瓶中有红褐色沉淀产生,但是没有观察到黄绿色气体产生.此时烧瓶中发生的氧化还原反应的离子方程式为
3ClO-+6Fe2++3H2O=2Fe(OH)3↓+4Fe3++3Cl-
3ClO-+6Fe2++3H2O=2Fe(OH)3↓+4Fe3++3Cl-
.(5)取100mL 0.1mol/L Ba(OH)2溶液,向其中逐滴加入同浓度的KHSO4溶液至Ba2+恰好完全沉淀,此时溶液的PH值为
10.7
10.7
(忽略两溶液混合时的体积变化,混合后溶液的温度为100℃,100℃时Kw=1x10-12)分析:(1)电解饱和食盐水得到氯气、氢气、氢氧化钠溶液,氯气和氢氧化钠溶液反应生成次氯酸钠和氯化钠溶液;氯气全部和氢氧化钠反应生成次氯酸钠溶液和氢气;次氯酸钠溶液水解显碱性;
(2)依据溶液中铝离子水解生成氢氧化铝和氢离子,质子守恒是水电离出的氢离子和氢氧根离子守恒;
(3)①烧瓶中加入饱和KAl(SO4)2溶液,次氯酸根离子水解显碱性,铝离子水解显酸性,混合后水解相互促进,产生大量的白色胶状沉淀和次氯酸;
②依据现象分析是次氯酸分解生成氯气、氧气和水的反应;
(4)亚铁离子具有还原性,次氯酸根离子教育氧化性在溶液中发生氧化还原反应,依据原子守恒和电子守恒计算书写离子方程式;
(5)Ba(OH)2溶液与KHSO4溶液至Ba2+恰好完全沉淀,反应物质的量之比为1:1,依据剩余溶液中氢氧根离子计算浓度结合Kw计算氢离子浓度计算溶液PH;
(2)依据溶液中铝离子水解生成氢氧化铝和氢离子,质子守恒是水电离出的氢离子和氢氧根离子守恒;
(3)①烧瓶中加入饱和KAl(SO4)2溶液,次氯酸根离子水解显碱性,铝离子水解显酸性,混合后水解相互促进,产生大量的白色胶状沉淀和次氯酸;
②依据现象分析是次氯酸分解生成氯气、氧气和水的反应;
(4)亚铁离子具有还原性,次氯酸根离子教育氧化性在溶液中发生氧化还原反应,依据原子守恒和电子守恒计算书写离子方程式;
(5)Ba(OH)2溶液与KHSO4溶液至Ba2+恰好完全沉淀,反应物质的量之比为1:1,依据剩余溶液中氢氧根离子计算浓度结合Kw计算氢离子浓度计算溶液PH;
解答:解:(1)电解饱和食盐水得到氯气、氢气、氢氧化钠溶液,氯气和氢氧化钠溶液反应生成次氯酸钠和氯化钠溶液;氯气全部和氢氧化钠反应生成次氯酸钠溶液和氢气;反应的离子方程式为:Cl-+H2O
ClO-+H2↑;次氯酸钠溶液水解显碱性;ClO-+H2O?HClO+OH-;故答案为:Cl-+H2O
ClO-+H2↑;大于;ClO-+H2O?HClO+OH-;
(2)液中铝离子水解生成氢氧化铝和氢离子,质子守恒是水电离出的氢离子和氢氧根离子守恒,c(H+)=c(OH-)+3c(Al(OH)3);故答案为:c(H+)=c(OH-)+3c(Al(OH)3);
(3)①烧瓶中加入饱和KAl(SO4)2溶液,次氯酸根离子水解显碱性,铝离子水解显酸性,混合后水解相互促进,产生大量的白色胶状沉淀和次氯酸,反应的离子方程式为:
3Cl-+Al3++3H2O=3HClO+Al(OH)3↓;故答案为:3Cl-+Al3++3H2O=3HClO+Al(OH)3↓;
②将烧瓶中的混合液在阳光照射下,不久烧瓶中有黄绿色气体产生为氯气,充分反应后集气瓶中收集到一种无色无味的气体为氧气.依据氧化还原反应电子守恒写出化学方程式配平得到:4HClO
2H2O+2Cl2↑+O2↑;
故答案为:4HClO
2H2O+2Cl2↑+O2↑;
(4)若将分液漏斗中的KAl(SO4)2溶液换成硫酸亚铁铵(一种复盐:(NH4)2SO4?FeSO4)溶液,其他不变.打开分液漏斗活塞向烧瓶中滴入足量的硫酸亚铁铵溶液.观察到烧瓶中有红褐色沉淀产生,但是没有观察到黄绿色气体产生,亚铁离子具有还原性,次氯酸根离子教育氧化性在溶液中发生氧化还原反应,
反应的离子方程式为:3ClO-+6Fe2++3H2O=2Fe(OH)3↓+4Fe3++3Cl-;
故答案为:3ClO-+6Fe2++3H2O=2Fe(OH)3↓+4Fe3++3Cl-;
(5)取100mL 0.1mol/L Ba(OH)2溶液,向其中逐滴加入同浓度的KHSO4溶液至Ba2+恰好完全沉淀,Ba(OH)2溶液与KHSO4溶液至Ba2+恰好完全沉淀,需要同浓度溶液体积为100ml,反应物质的量之比为1:1,剩余氢氧根离子物质的量为0.01mol,浓度c(OH-)=
=0.05mol/L;100℃时Kw=1x10-12,c(H+)=
=2×10-11mol/L;PH=-lg2×10-11mol/L=10.7,故答案为:10.7;
| ||
| ||
(2)液中铝离子水解生成氢氧化铝和氢离子,质子守恒是水电离出的氢离子和氢氧根离子守恒,c(H+)=c(OH-)+3c(Al(OH)3);故答案为:c(H+)=c(OH-)+3c(Al(OH)3);
(3)①烧瓶中加入饱和KAl(SO4)2溶液,次氯酸根离子水解显碱性,铝离子水解显酸性,混合后水解相互促进,产生大量的白色胶状沉淀和次氯酸,反应的离子方程式为:
3Cl-+Al3++3H2O=3HClO+Al(OH)3↓;故答案为:3Cl-+Al3++3H2O=3HClO+Al(OH)3↓;
②将烧瓶中的混合液在阳光照射下,不久烧瓶中有黄绿色气体产生为氯气,充分反应后集气瓶中收集到一种无色无味的气体为氧气.依据氧化还原反应电子守恒写出化学方程式配平得到:4HClO
| ||
故答案为:4HClO
| ||
(4)若将分液漏斗中的KAl(SO4)2溶液换成硫酸亚铁铵(一种复盐:(NH4)2SO4?FeSO4)溶液,其他不变.打开分液漏斗活塞向烧瓶中滴入足量的硫酸亚铁铵溶液.观察到烧瓶中有红褐色沉淀产生,但是没有观察到黄绿色气体产生,亚铁离子具有还原性,次氯酸根离子教育氧化性在溶液中发生氧化还原反应,
反应的离子方程式为:3ClO-+6Fe2++3H2O=2Fe(OH)3↓+4Fe3++3Cl-;
故答案为:3ClO-+6Fe2++3H2O=2Fe(OH)3↓+4Fe3++3Cl-;
(5)取100mL 0.1mol/L Ba(OH)2溶液,向其中逐滴加入同浓度的KHSO4溶液至Ba2+恰好完全沉淀,Ba(OH)2溶液与KHSO4溶液至Ba2+恰好完全沉淀,需要同浓度溶液体积为100ml,反应物质的量之比为1:1,剩余氢氧根离子物质的量为0.01mol,浓度c(OH-)=
| 0.01mol |
| 0.2L |
| 10-12 |
| 0.05 |
点评:本题考查了电解原理的应用,反应产物判断,盐类水解的应用,氧化还原反应的分析判断,溶液PH计算应用,题目难度中等.

练习册系列答案
相关题目
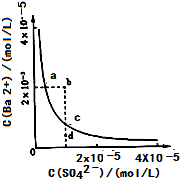 (2013?达州模拟)难溶物BaSO4在水中的溶解平衡可表示为:BaSO4(s)?Ba2+(aq)+SO42-(aq).其溶度积常数Ksp=C(Ba2+)?C(SO42-),某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
(2013?达州模拟)难溶物BaSO4在水中的溶解平衡可表示为:BaSO4(s)?Ba2+(aq)+SO42-(aq).其溶度积常数Ksp=C(Ba2+)?C(SO42-),某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )