题目内容
【题目】下列说法中错误的是( )
A.钠在常温下就容易被氧化B.钠受热后能够着火燃烧
C.钠在空气中缓慢氧化能自燃D.钠在氧气中燃烧比在空气中燃烧剧烈
【答案】C
【解析】
A.钠在常温下就容易被空气中的氧气氧化为Na2O,A不合题意;
B.钠在空气中受热后能够着火燃烧,生成Na2O2,B不合题意;
C.钠在空气中缓慢氧化,生成Na2O,但不能自燃,C符合题意;
D.空气中O2的浓度小于氧气,所以钠在氧气中燃烧比在空气中剧烈,D不合题意;
故选C。

 阅读快车系列答案
阅读快车系列答案【题目】五种短周期主族元素 W、M、X、Y、Z 原子序数依次增大,请结合表中信息回答下列问题:
元素 | W | M | X | Y | Z |
结构或性质 | 最高价含氧 酸与其气态 氢化物能发 生化合反应 | 氢化物的水 溶液能刻蚀 玻璃 | 焰色反应火 焰呈黄色 | 同周期主族元 素形成的简单 离子中,其离子 半径最小 | 最高正价与 最低负价代 数和为 6 |
(1)M元素在周期表中的位置为_____。
(2)M、X、Z元素所对应简单离子半径由大到小的顺序为_____________________(用离子符号表示)。
(3)W最高价含氧酸与其气态氢化物发生化合反应生成的物质中含有的化学键类型为___________________________________。
(4)下列可作为比较M和Z的非金属性强弱的依据是_________(填序号)。
A.单质与H2反应的难易程度
B.氢化物的稳定性
C.最高价氧化物的水化物酸性强弱
D.将M的单质通入Z的钠盐溶液观察是否有Z逸出
(5)W能形成多种氢化物,其中一种氢化物可作为火箭燃料,该物质中W与氢元素的质量比为7:1,写出该氢化物的电子式______。该氢化物和 O2 在碱性条件下可形成燃料电池,产生两种无毒物质,写出其负极的电极反应式___________.
(6)Y元素和W元素形成的化合物YW一种新型无机材料,可与过量烧碱溶液反应产生使湿润的红色石蕊试纸变蓝的气体,写出有关的化学方程式_______。
【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.01. | 0.008 | 0.007 | 0.007 | 0.007 |
(1)已知:K300℃>K350℃,写出该反应的平衡常数表达式:K=_________________,关于该反应的下列说法中,正确的是________。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
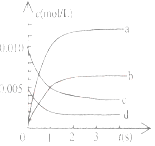
(2)下图中表示NO2的变化的曲线是____________________,用O2表示从0-2s内该反应的平均速率v=_______________。
(3)能说明该反应已达到平衡状态的是__________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v (NO)=2v(O2) D.容器内密度保持不变
(4)下列措施中能使n(NO2)/n(NO)增大的有____。(填字母)
A.升高温度 B.加入催化剂
C.不断充入O2 D.充入He(g),使体系总压强增大