题目内容
8.①有尘埃的空气、②溴水、③蒸馏水、④沸水中加几滴FeCl3浓溶液、⑤淀粉溶液,其中不存在丁达尔效应的分散系是( )| A. | ② | B. | ②③⑤ | C. | ②③ | D. | ①②③⑤ |
分析 根据胶体能够发生丁达尔现象,只要在选项中判断分散系是否是胶体即可作答.
解答 解:①有尘埃的空气为胶体,具有丁达尔效应,故①错误;
②溴水为溶液,不是胶体,不具有丁达尔效应,故②正确;
③蒸馏水不是胶体,不具有丁达尔效应,故③正确;
④沸水中加几滴FeCl3浓溶液可制得氢氧化铁胶体,具有丁达尔效应,故④错误;
⑤淀粉溶液为胶体,具有丁达尔效应,故⑤错误;
故选C.
点评 本题考查了胶体的性质,比较简单,只要准确掌握胶体性质即可作答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18. 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
1.00.50t(s)123c(mol/L)abcd
(1)已知升高温度,NO2的浓度减小,则该反应是放热反应.
(2)图中表示NO2的变化的曲线是b
用O2表示从0~2s内该反应的平均速率v=0.15mol/(L•s)
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是c
a.及时分离除NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂.
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 2.0 | 1.0 | 0.8 | 0.7 | 0.7 | 0.7 |
(1)已知升高温度,NO2的浓度减小,则该反应是放热反应.
(2)图中表示NO2的变化的曲线是b
用O2表示从0~2s内该反应的平均速率v=0.15mol/(L•s)
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是c
a.及时分离除NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂.
16.用X、Y、Z、w四种金属进行如下实验:
根据以上事实.下列判断或推测错误的是( )
| 1 | 将X与Y用导线连接,浸入电解质溶液中,Y极上有气泡产生 |
| 2 | 将片状X、W分别投入等浓度的稀盐酸中都有气体产生,W比X反应剧烈 |
| 3 | 用惰性电极电解等物质的量浓度的Y和Z的硝酸盐混合溶液,在阴极上首先析出Z |
| A. | 上述四种金属中,Z的单质还原性最弱 | |
| B. | w的还原性强于Y的还原性 | |
| C. | Z放人CuSO4溶液中一定有Cu析出 | |
| D. | 用X、Z和稀硫酸可构成原电池,X作负极 |
17.下列叙述不正确的是( )
| A. | 除去镁粉中少量的铝粉,加足量氢氧化钠溶液反应后,过滤 | |
| B. | 做水的蒸馏实验时,要在烧瓶内加几粒沸石以防止暴沸 | |
| C. | 金属钠可以保存在煤油里 | |
| D. | 可用过滤的方法除去氢氧化铁胶体中的氯化铁溶液 |
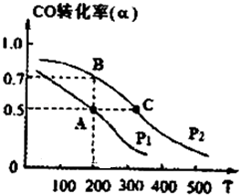 工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol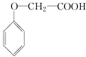 发生化学反应的产物.
发生化学反应的产物. 、
、 等.
等.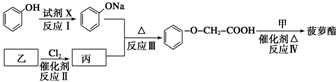
 .
.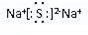 ,所含化学键类型离子键;
,所含化学键类型离子键;