题目内容
(12分) A、B、C、D、E、F、G七种元素,试按下列所给条件推断,①A、B、C是同一周期的金属元素,原子核外有三个电子层,A的原子半径在所属周期中最大,且原子半径A>B>C;②D、E是非金属元素,它们跟氢气化合可生成气态氢化物HD和HE,室温时,D的单质是液体,E的单质是固体
③F在常温下是气体,性质稳定,是除氢气外最轻的气态④G是除氢外原子半径最小的元素
(1)A 的名称是 ,B位于周期表中第 周期第 族,C的原子结构示意图是
(2)A元素与D元素形成化合物的电子式是
(3)F的元素符号是
(4)在上述七种元素中,最高价氧化物对应的水化物碱性最强的化学式是 ,酸性最强的化学式是 ,气态氢化物最稳定的化学式是
(5)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中,反应的化学方程式是
③F在常温下是气体,性质稳定,是除氢气外最轻的气态④G是除氢外原子半径最小的元素
(1)A 的名称是 ,B位于周期表中第 周期第 族,C的原子结构示意图是
(2)A元素与D元素形成化合物的电子式是
(3)F的元素符号是
(4)在上述七种元素中,最高价氧化物对应的水化物碱性最强的化学式是 ,酸性最强的化学式是 ,气态氢化物最稳定的化学式是
(5)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中,反应的化学方程式是
(1)钠 第三周期 第ⅡA族 铝原子结构示意图 (2)溴化钠电子式
(2)溴化钠电子式 (3)He (4) NaOH HBrO4 HF (5)Al(OH)3+NaOH =NaAlO2+2H2O
(3)He (4) NaOH HBrO4 HF (5)Al(OH)3+NaOH =NaAlO2+2H2O
 (2)溴化钠电子式
(2)溴化钠电子式 (3)He (4) NaOH HBrO4 HF (5)Al(OH)3+NaOH =NaAlO2+2H2O
(3)He (4) NaOH HBrO4 HF (5)Al(OH)3+NaOH =NaAlO2+2H2O试题分析:根据题意可推知这几种元素分别是:A是Na;B是Mg;C是Al;D是Br;E是I;F是He;G是F。(1)A 的名称是钠;B元素是Mg。位于周期表中第三周期第ⅡA族;C元素是Al。其结构示意图为:
 。(2)Na与Br2形成化合物NaBr的电子式是
。(2)Na与Br2形成化合物NaBr的电子式是 。(3)F元素是氦,其元素符号是He。(4)在上述七种元素中,元素的金属性最强的是Na,所以最高价氧化物对应的水化物碱性最强的是NaOH。非金属性最强的元素是F,但是F无含氧酸。除此之外非金属性最强的是Br,酸性最强的化学式是HBrO4;非金属性最强的元素是F,元素的非金属性越强,其对应的气态氢化物的稳定性也越强。所以最稳定的化学式是HF。(5)Al(OH)3是两性氢氧化物,能与强酸、强碱发生反应。Al(OH)3与NaOH反应的化学方程式为:Al(OH)3+NaOH =NaAlO2+2H2O。
。(3)F元素是氦,其元素符号是He。(4)在上述七种元素中,元素的金属性最强的是Na,所以最高价氧化物对应的水化物碱性最强的是NaOH。非金属性最强的元素是F,但是F无含氧酸。除此之外非金属性最强的是Br,酸性最强的化学式是HBrO4;非金属性最强的元素是F,元素的非金属性越强,其对应的气态氢化物的稳定性也越强。所以最稳定的化学式是HF。(5)Al(OH)3是两性氢氧化物,能与强酸、强碱发生反应。Al(OH)3与NaOH反应的化学方程式为:Al(OH)3+NaOH =NaAlO2+2H2O。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
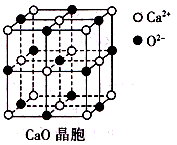
 ,每个晶胞中分摊2个钾原子
,每个晶胞中分摊2个钾原子 Rx[CrCln(H2O)6-n]+xH+。将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1NaOH溶液25.00 mL,则该配离子的化学式为_______。
Rx[CrCln(H2O)6-n]+xH+。将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1NaOH溶液25.00 mL,则该配离子的化学式为_______。