题目内容
【题目】下图,两电极上发生的电极反应分别为:a极:Ag++e-=Ag b极:Fe-2e-=Fe2+
下列说法正确的是( )
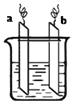
A. a极材料一定为金属银
B. b极一定连电源的正极
C. 装置中电解质溶液阳离子一定只含有Ag+
D. 装置中发生的反应方程式一定是Fe +2Ag+===Fe2++2Ag
【答案】D
【解析】a极:2Ag++2e-=2Ag,说明银离子在a极上得电子发生还原反应,电解质溶液中一定含有银离子;b极:Fe-2e-=Fe2+,说明铁作负极或阳极,失电子发生氧化反应,正极或阴极材料可以是比铁活泼性差的金属或非金属。A.a极材料可以是比铁活泼性差的金属或非金属,不一定是银,故A错误;B.该装置可能为原电池,b极是铁发生失电子的氧化反应,则b极为负极,故B错误;C.银离子得电子发生还原反应,电解质溶液中一定含有银离子,可能含有其他阳离子,如钠离子,故C错误;D.由a、b电极上的电极反应可知,发生的反应为Fe+2Ag+=Fe2++2Ag,故D正确;故选D。

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目