题目内容
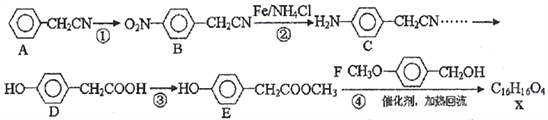
【题目】有机物X 是某种药物的主要成分,工业上合成该化合物的一种路线如下(部分反应物、反应条件略去):
已知:酯与含羟基的化合物可发生如下酯交换反应:![]() (其中R、
(其中R、![]() 、
、![]() 均代表烃基)
均代表烃基)
(1)反应①所需反应条件是_______________,反应②的反应类型是________________。
(2)E中官能团的名称是_____________; 反应④的产物除了X以外。另一种产物的名称是_________。
(3)D在一定条件下能发生缩聚反应生成高分子化合物,该高分子化合物的结构简式为_____________。
(4)反应③的化学方程式为_____________________________。
(5)D的同分异构体有多种,写出符合下列条件的有机物结构简式____________。
Ⅰ.苯环上一氯代物只有一种
Ⅱ.与氯化铁溶液发生显色反应
Ⅲ.能与新制Cu(OH)2悬浊液共热产生红色沉淀
Ⅳ.1mol该物质与足量的钠充分反应产生标准状况下22.4LH2
(6)已知:
①![]() ;
;
②当苯环上已有一个“-CH3”或“-Cl”时,新引入的取代基一般在它的邻位或对位;当苯环上已有一个“-NO2”或“-COOH”时,新引入的取代基一般在它的间位。
请写出以甲苯、乙醇为原料制备 的合成路线图(无机试剂任用)___________。
的合成路线图(无机试剂任用)___________。
【答案】 浓硫酸,(水浴)加热 还原反应 羟基、醚键 “甲醇”、“木精”或者“木醇” 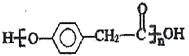
![]()
 或
或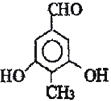
【解析】A与浓硫酸、浓硝酸的混合溶液加热发生硝化反应生成B,B中的硝基发生还原反应生成C;D分子中含有羧基,与甲醇发生酯化反应生成E;根据X的分子式可判断E与F发生的是酯基的交换反应生成X和甲醇,则X的结构简式为![]() 。
。
(1)A与浓硫酸、浓硝酸的混合溶液加热发生硝化反应生成B。反应②的反应类型是还原反应,故答案为:浓硫酸,(水浴)加热;还原反应;
(2)E(![]() )中官能团有羟基、醚键;根据X的分子式可判断反应④中E与F发生的是酯基的交换反应生成X和甲醇,故答案为:羟基、醚键;甲醇;
)中官能团有羟基、醚键;根据X的分子式可判断反应④中E与F发生的是酯基的交换反应生成X和甲醇,故答案为:羟基、醚键;甲醇;
(3)D在一定条件下能发生缩聚反应生成高分子化合物,该高分子化合物的结构简式为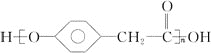 。
。
(4)反应③是D与甲醇发生的酯化反应,反应的化学方程式为![]() +CH3OH
+CH3OH![]()
![]() +H2O,故答案为:
+H2O,故答案为:![]() +CH3OH
+CH3OH![]()
![]() +H2O;
+H2O;
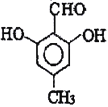
(5) D为![]() ,Ⅰ.苯环上一氯代物只有一种;Ⅱ.与氯化铁溶液发生显色反应,说明含有酚羟基;Ⅲ.能与新制Cu(OH)2悬浊液共热产生红色沉淀,说明含有醛基;Ⅳ.1mol 该物质与足量的钠充分反应产生标准状况下22.4LH2即1mol氢气,说明结构中含有2个羟基;满足条件的有
,Ⅰ.苯环上一氯代物只有一种;Ⅱ.与氯化铁溶液发生显色反应,说明含有酚羟基;Ⅲ.能与新制Cu(OH)2悬浊液共热产生红色沉淀,说明含有醛基;Ⅳ.1mol 该物质与足量的钠充分反应产生标准状况下22.4LH2即1mol氢气,说明结构中含有2个羟基;满足条件的有 或
或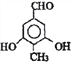 ,故答案为:
,故答案为: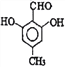 或
或 ;
;
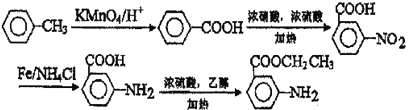
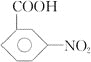
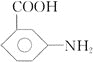
(6) 以甲苯、乙醇为原料制备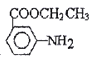 。要合成间-氨基苯甲酸乙酯,则首先要利用甲苯的氧化反应生成苯甲酸,然后利用苯甲酸的取代反应引入硝基,再把硝基还原为氨基,最后与乙醇发生酯化反应即可,合成路线可设计为:
。要合成间-氨基苯甲酸乙酯,则首先要利用甲苯的氧化反应生成苯甲酸,然后利用苯甲酸的取代反应引入硝基,再把硝基还原为氨基,最后与乙醇发生酯化反应即可,合成路线可设计为:![]()
![]()
![]()
![]()
![]()
![]()
 ,故答案为:
,故答案为:![]()
![]()
![]()
![]()

![]()

![]()
 。
。

【题目】有六种短周期元素,已知A的单质是最清洁的能源物质,其他元素的原子半径及主要化合价如下表:
元素代号 | B | C | D | E | F |
原子半径/nm | 0.186 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +1 | +3 | +6、-2 | +7、-1 | -2 |
根据上述信息回答以下问题。
(1)D在元素周期表中的位置______________;E的离子结构示意图______________。
(2)关于A元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,试分析其理由________________________________。
(3)用电子式表示B的单质与D的单质形成化合物的过程________________________。
(4)下列各项比较,正确的是________________________。
①氢化物的沸点:D低于F ②A~F元素的简单离子半径:C的最大
③气态氢化物稳定性:D比E稳定 ④最高价氧化物对应的水化物碱性:B小于C
(5)E单质常用于自来水消毒。用必要的文字和离子方程式解释原因______________________________________________________________。
(6)写出C的单质与B的最高价氧化物的水化物反应的离子方程式________________。
(7)C的单质与元素M的红棕色氧化物N反应可用于焊接钢轨,该反应的化学方程式为________________________________。
(8)已知单质M的燃烧热为375kJ/mol,写出表示其燃烧热的热化学方程式___________________________。
(9)已知NH3结合质子的能力强于F的氢化物,请用最恰当的离子方程式证明这个结论________________________________。