题目内容
【题目】我国科学家设计了一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时可除去酸性废水中的硝酸盐。下列说法正确的是
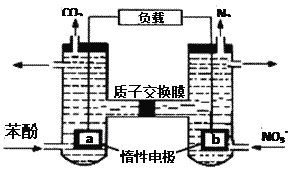
A. a极的电极反应式为C6H6O+11H2O + 28e-=6CO2↑ + 28H+
B. 外电路电子移动方向由b极到a极
C. 若正极产生5.6L气体(标况下),则转移电子2.5mol
D. 电池工作一段时间后,左池溶液的pH增大
【答案】C
【解析】A.该原电池中,硝酸根离子得电子发生还原反应,则右边装置中电极b是正极,电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,左边装置电极a是负极,负极上C6H6O失电子发生氧化反应生成二氧化碳,电极反应式为C6H6O+11H2O-28e-=6CO2↑+28H+,A错误;B.外电路电子移动方向由a极到b极,B错误;C.右边装置中电极b是正极,电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,产生5.6L气体(标况下),即产生氮气是0.25mol,则转移电子0.25mol×10=2.5mol,C正确;D.左边装置电极a是负极,负极上C6H6O失电子发生氧化反应生成二氧化碳,电极反应式为C6H6O+11H2O-28e-=6CO2↑+28H+,因此电池工作一段时间后,左池溶液的pH减小,D错误;答案选C。

练习册系列答案
相关题目