题目内容
含有农药、染料、酚、氰化物,以及引起色度、臭味的废水,常用化学氧化法进行处理,所用的氧化剂有氯类(如液氯、次氯酸钙、次氯酸钠等)和氧类(如空气、臭氧、过氧化氢、高锰酸钾等)。一个典型实例是用氯氧化法处理含有剧毒的氰化物(含CN-)的废水。在碱性条件下(pH=8.5~11),氯气可将氰化物中CN-氧化为只有它毒性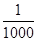 的氰酸盐(含CNO-)。
的氰酸盐(含CNO-)。
(1)写出含CN-废水用氯气氧化生成氰酸盐的离子方程式:________________________________________________________________。
(2)若向含CNO-的废水中再通入氯气,可使CNO-转化为无毒的气体,写出这个反应的离子方程式:______________________________________________。
(3)在用液氯不便的地区,可用漂白粉处理含CN-的废水,若将其氧化为CNO-,其离子方程式为__________________________________________。
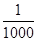 的氰酸盐(含CNO-)。
的氰酸盐(含CNO-)。(1)写出含CN-废水用氯气氧化生成氰酸盐的离子方程式:________________________________________________________________。
(2)若向含CNO-的废水中再通入氯气,可使CNO-转化为无毒的气体,写出这个反应的离子方程式:______________________________________________。
(3)在用液氯不便的地区,可用漂白粉处理含CN-的废水,若将其氧化为CNO-,其离子方程式为__________________________________________。
(1)CN-+Cl2+2OH-=CNO-+2Cl-+H2O
(2)2CNO-+3Cl2+8OH-=2CO32-+6Cl-+4H2O+N2
(3)CN-+ClO-=CNO-+Cl-
(2)2CNO-+3Cl2+8OH-=2CO32-+6Cl-+4H2O+N2
(3)CN-+ClO-=CNO-+Cl-
(1)CN-是在碱性条件下被Cl2氧化的,故反应物应有OH-参加,产物除生成氰酸盐外还应有Cl-及H2O,离子方程式为CN-+Cl2+2OH-=CNO-+2Cl-+H2O。
(2)当Cl2过量时(1)中的产物CNO-与Cl2反应,碱性条件下不可能产生CO2及其他气体,而碳元素的存在形式为CO32-,无毒气体一定为N2,离子方程式:2CNO-+3Cl2+8OH-=2CO32-+6Cl-+4H2O+N2。
(3)由于漂白粉中的ClO-具有强氧化性,故可发生反应:CN-+ClO-=CNO-+Cl-。
(2)当Cl2过量时(1)中的产物CNO-与Cl2反应,碱性条件下不可能产生CO2及其他气体,而碳元素的存在形式为CO32-,无毒气体一定为N2,离子方程式:2CNO-+3Cl2+8OH-=2CO32-+6Cl-+4H2O+N2。
(3)由于漂白粉中的ClO-具有强氧化性,故可发生反应:CN-+ClO-=CNO-+Cl-。

练习册系列答案
相关题目
 2Cu+O2↑+4H+
2Cu+O2↑+4H+
 Cl2
Cl2